1. 서 론
2. 재료 및 방법
2.1 M. aeruginosa 배양
2.2 초음파 (Ultrasonic) 발생장치 구성
2.3 초음파를 활용한 M. aeruginosa 성장억제
2.4 시료 분석방법
3. 결과 및 고찰
3.1 초음파 적용 시간에 따른 육안 변화
3.2 Chlorophyll-a와 M. aeruginosa의 개체수 변화
3.3 성장률과 일차분해율 분석
3.4 초음파에 의한 M. aeruginosa의 형태학적 변화
4. 결 론
1. 서 론
녹조 (algal bloom)현상은 부영양화된 정체수역에서 조류의 대량발생으로 수체로의 햇빛차단, 용존산소 감소, 독소에 의한 어류 폐사 등 생태학적인 불균형을 유발하며 물의 심미적 가치와 안전성을 저감시킨다 (Kim et al. 2015, Byeon et al. 2018, Paerl and Barnard 2020, Hallegraeff et al 2021). 최근에는 기후변화 (climate change)에 따른 수온의 지속적 상승과 도시화 및 산업화로 인한 과도한 영양염류 [질소 (N), 인 (P)]의 수계 유입과 더불어 수계 내 설치된 다양한 인공 구조물에 의한 정체수역 증가 등의 영향으로 조류가 과다 증식하여 녹조현상의 발생빈도 및 강도가 점점 증가하는 추세이다 (Thackeray et al. 2008, Lee and Lee 2012, Kim et al. 2019, Jang et al. 2021, Meerhoff et al. 2022). 우리나라 수계에서 녹조현상 발생 시 가장 흔하게 문제를 일으키는 남조류인 Microcystis aeruginosa (M. aeruginosa)의 경우 군체 (colony)를 형성하고, 기낭 (gas vesicle)이 있어 일주성 수직이동 등의 특성이 있으며, 수계 내 독성물질인 마이크로시스틴 (microcystin)을 배출하여 수생태계 위해성을 유발하여 수자원으로서의 가치를 하락시킨다 (Oh et al. 2001, Codd et al. 2005, Park et al. 2011, Lee et al. 2013, Harke et al. 2016).
이러한 문제점을 야기하는 유해남조류 (Harmful cyanobacteria)의 저감을 위해 최근 연구되어지고 있는 다양한 공법들 중 물리적 공법인 초음파 (ultrasonic)를 활용한 조류 저감 기술은 초음파의 공동현상 (cavitation)으로 남조류의 미세소기관인 기낭을 파괴하여 조류의 부력조절 능력을 상실시켜 호소 바닥에 가라앉게 하고, 빛을 이용한 광합성작용을 차단함으로써 남조류의 생장을 억제하는 기술이다 (Ahn et al. 2003, Jachlewski et al. 2013, Park et al. 2013, Purcell et al. 2013, Song 2014, Park et al. 2017, Kong et al. 2019, Jang et al. 2022). 또한 초음파는 기낭 파괴를 통한 조류 저감뿐만 아니라 남조류의 세포분열을 억제하여 조류대발생을 예방하고, 남조류가 발생하는 독성물질 (microcystin)의 분해에 효과가 있다고 보고되고 있다 (Ma et al. 2005, Srisuksomwong et al. 2011, Dehghani 2016, Chen et al. 2020). 이러한 초음파를 이용한 기법은 화학약품의 수체 내 주입을 필요로 하지 않아 2차 오염을 유발하지 않으며 수생태계의 위해성이 낮은 친환경적 처리 공법인 동시에 남조류의 생장억제 효과를 얻을 수 있다.
초음파를 활용한 조류 저감을 위하여 기존 선행 연구에서는 초음파의 주파수 (frequency), 출력 (watt), 조사시간 (irradiation time)에 따른 유해남조류의 성장억제에 관한 다양한 연구가 진행되어 왔다. Wu et al. (2012)은 주파수가 낮을수록 M. aeruginosa의 성장억제에 효율이 높게 (20 kHz > 580 kHz > 1146 kHz) 도출된다고 보고하였으며, Sim et al. (2006)과 Zhang et al. (2006), Rajasekhar et al. (2012)은 초음파의 출력이 높을수록, 조사시간이 길어질수록 조류 성장억제 효율이 높은 것을 확인하였다. 하지만 이러한 연구들 대부분은 주로 1.5 L 미만의 소량의 시료로 실험이 진행되었고, 단기간의 초음파 조사에 의한 조류 성장억제 효율을 확인하였으며, 일시적인 조류 성장억제 효과는 관찰하였으나 대규모 수체에서의 장기적 조류 성장억제 효과를 확인하지 못했다는 한계를 가지고 있다.
따라서 본 연구에서는 녹조현상의 주요 원인종인 M. aerginosa 단일종의 시료를 기존 연구 대비 대용량 (10 L) 시료를 활용하여 현장 mesocosm과 유사한 실험실 규모 (lab-scale) 실험을 진행하였으며, 선행연구 (Jang et al. 2022)에서 도출된 최적의 초음파 조사 조건 기반 다양한 초음파 조사시간별 M. aeruginosa의 성장억제 효과를 조사하였다. 또한 초음파의 조류 성장억제 효과를 검증하고 초음파 조사 종료 후 조사시간에 따른 조류의 재성장 주기 (regrowth period)를 도출하기 위해 (1) 초음파 적용 시간에 따른 시료의 육안 변화, (2) Chlorophyll-a (Chl-a)와 M. aeruginosa 개체수 변화, (3) M. aeruginosa 개체수 기반 비성장속도 (μ) 및 일차분해속도 (κ) 산출, (4) 주사전자현미경 (SEM) 및 투과전자현미경 (TEM) 분석을 통한 M. aeruginosa의 세포 표면 및 내부 형질 변화를 분석하였다. 이러한 검증 결과를 종합해 초음파 조사시간별 조류의 성장억제 효율 (efficiency)과 지속성 (sustainability)을 확인하였다.
2. 재료 및 방법
2.1 M. aeruginosa 배양
실험 조류인 남조류 M. aeruginosa는 경기도 W저수지로부터 채수하여 실험실에서 동정 분리하였다. M. aeruginosa 배양은 CB 배지를 사용하였으며, pH 9로 조정한 CB 배지와 일정량의 M. aeruginosa를 접종하여 표면적 182.5 cm2, 부피 500 mL의 cell culture 플라스크 (VWR, Co., America)에 담아 계대배양 (subculture)하였다. CB 배지의 구체적인 성분은 Jang et al. (2021)에 제시되었다.
배양조건은 온도 27±1°C, 광량 12 μmol-photons m-1 s-1, 광주기 12 hr :12 hr (light : dark) cycle, 회전속도 28±1 rpm의 조건을 갖춘 조류배양장치에서 약 30일간 배양하여 실험에 사용하였다.
2.2 초음파 (Ultrasonic) 발생장치 구성
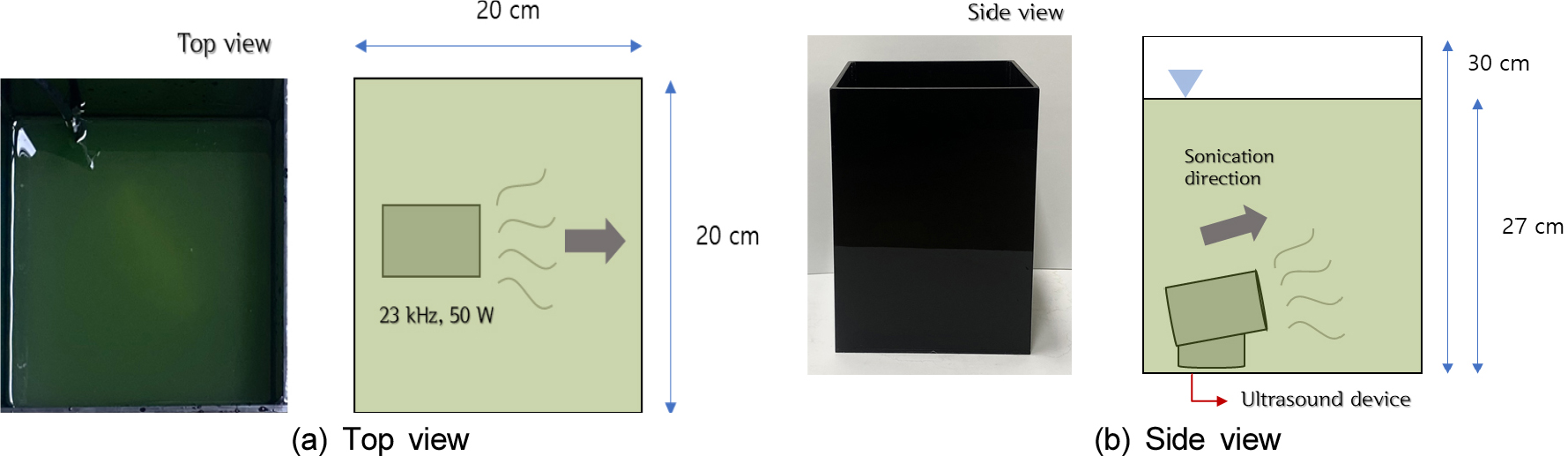
초음파 조사조건 변화에 따른 M. aeruginosa의 성장억제에 미치는 영향 비교 및 분석을 위하여 초음파 발생장치와 진동판 구동회로를 직접 조합하여 제작하였다 (AD Sonic, Co., Korea). 본 실험에서 사용한 초음파 발생장치의 진동판은 9.6 cm2 크기의 Hainertec Co. (China) 제품을 활용하였으며, 23 kHz의 고정 주파수가 발생하도록 조정하였다. 그리고 출력은 전원공급장치를 통해 50 W의 고정 출력으로 초음파가 발생하도록 조절하여 실험에 적용하였다.
2.3 초음파를 활용한 M. aeruginosa 성장억제
본 실험에서는 Fig. 1에 제시되었듯, 20 cm (L)×20 cm (W)×30 cm (H) 규격의 차광된 아크릴 반응조 (acrylic reactor)를 사용하였으며, 기존 연구 대비 비교적 대용량인 10 L의 M. aeruginosa 시료를 사용하여 실험을 진행하였다. 초음파 조사 조건은 이전 연구 (Jang et al. 2022)에서 도출된 초음파 조사 조건 (주파수 23 kHz, 출력 6.94 W L-1)을 활용하여 각 실험 조건별로 1회 초음파 조사 실험을 진행하였다. 본 연구에서는 초음파 조사시간에 따른 M. aeruginosa의 성장억제 효과를 비교 ․ 분석하기 위해 다양한 시간별 [0 hr (T_A), 0.5 hr (T_B), 1 hr (T_C), 1.5 hr (T_D), 2 h r (T_E), 2.5 hr (T_F), 3 hr (T_G)]로 초음파 조사를 실시하였으며 초음파 조사 종료 후 채수를 진행하였다. 시료 채수 시 시료를 충분히 교반 후 채수하였으며, 채수로 인한 부피 변화로 단위 부피당 조사에너지의 변화를 방지하기 위해 채수 후 출력 (Watt)을 조절하여 실험기간 동안 일정한 단위 부피당 조사 에너지 (Watt L-1)를 유지하였다. 채수한 시료는 일정시간 (10 min) 침전 후 표층수로부터 2 cm 미만의 상등액의 Chl-a 및 세포수를 측정하였다. 본 연구의 초기 M. aeruginosa의 농도는 선행연구에서 초기 조류의 농도가 높을수록 초음파에 의한 조류 성장억제 효과가 명확하게 관측되는 것으로 확인되어 (Lee et al. 2018, Jang et al. 2022), 조류경보제 발령 기준 조류대발생 남조류 농도 (1 × 106 cells mL-1) 보다 높은 농도 (4.8 × 106 cells mL-1)를 실험에 적용하였다.
2.4 시료 분석방법
2.4.1 M. aeruginosa 개체수 분석
초음파 조사가 M. aeruginosa에 미치는 영향을 관찰하기 위해 혈구계수기 (Marienfeld, Germany)를 이용하여 M. aeruginosa의 개체수 (cell number)를 광학현미경 (DN-10A, Samwon Scientific Industries, Ltd., Korea)으로 직접 계수하였다. 개체수 측정은 루골용액 (lugol’s iodine solution)으로 고정한 일정량의 시료를 혈구계수기에 넣고 눈금 안에 보이는 개체수를 현미경으로 측정하여 단위 부피당 개체수 (cells mL-1)를 계산하는 혈구계수법 (hemocytometry)을 사용하여 분석을 진행하였다. 또한 초음파 조사에 따른 개체수의 변화를 통해 M. aeruginosa의 비성장률 (specific growth rate)및 일차분해속도 (first order decay rate)를 도출하였으며, 다음의 식 Eq. 1과 Eq. 2를 이용하여 계산하였다.
여기서 µ는 비성장속도 (hr-1), k는 일차분해속도상수 (hr-1), N0는 초기 M. aeruginosa의 개체수 (cells mL-1) (t = 0), Nt는 일정시간 (t) 경과 후 M. aeruginosa의 개체수 (cells mL-1), 그리고 t는 경과시간 (hr)을 나타낸다.
2.4.2 초음파에 의한 M. aeruginosa의 형태학적 변화 분석
초음파 조사 전후의 M. aeruginosa의 형태학적 변화를 분석하고 비교하기 위해 주사전자현미경 (scanning electron microscopy, SEM)과 투과전자현미경 (transmission electron microscopy, TEM)을 활용하여 분석을 진행하였다. SEM 분석을 위해 남조류 시료를 전자현미경 고정액 (Karnovsky’s fixative)을 포함하여 5 mL로 12시간 동안 고정하였으며, poly-L-lysine (Ted pella, USA) 코팅된 10 mm 커버글라스에 2시간 부착시켜 0.1 M phosphate buffer로 세정하였다. 세정 후 ethyl alcohol로 탈수하였으며 1.5시간 동안 건조를 진행하였다. 건조된 시료는 lon coater (EM-ACE600, Leica, USA)를 이용하여 백금 (Pt) 코팅 후 FE-SEM (field emission scanning electron microscope)인 MAIA3 (TESCAN, Czech)를 사용해 10 kV의 가속전압에서 M. aeruginosa의 세포 표면을 관찰하였다. TEM 분석 또한 탈수과정까지의 전처리는 SEM 분석과 동일하게 진행되었으며, 100% ethyl alcohol와 LR White resin을 2:1, 1:1, 1:2로 혼합한 용액을 6시간 간격으로 치환하여 침투시켜 gelatin capsules에 시료와 LR White resin 용액을 넣고 밀봉하여 60°C 오븐에서 18시간 경화시켰다. 그 후 ultramicrotome (EM-UCT, Leica, USA)에 유리 나이프를 장착해 관찰할 범위를 결정 후 다이아몬드 나이프로 절편을 제작하였으며 5% uranyl acetate와 0.5% lead citrate를 이용해 이중염색하였다. 염색된 시료는 건조 후 TEM JEM-1010 (JEOL, Japan)을 이용하여 80 kV 가속전압에서 M. aeruginosa의 내부 단면을 관찰하였다.
3. 결과 및 고찰
3.1 초음파 적용 시간에 따른 육안 변화
초음파 조사시간별 M. aeruginosa의 성장억제에 미치는 영향을 비교 및 분석하기 위해 조사시간을 0 hr (T_A), 0.5 hr (T_B), 1 hr (T_C), 1.5 hr (T_D), 2 hr (T_E), 2.5 hr (T_F), 3 hr (T_G)로 실시한 후 31일간 M. aeruginosa의 변화를 관찰하였다. 시료의 육안상 변화를 관찰한 결과 (Fig. 2), 대조군 (T_A)은 관찰기간 (t ≤ 31 day) 동안 조류 특유의 녹색과 부유성이 지속적으로 증가하였으며, 실험 시작 후 31일 후에는 조류의 과다 성장으로 시료의 색이 매우 짙은 녹색으로 변화하는 것을 확인하였다 (Fig. 2 (a)). 실험군 (T_B, T_C, T_D, T_E, T_F, T_G)은 초음파 조사시간이 증가할수록 부유하는 M. aeruginosa 대비 침전된 M. aeruginosa의 증가로 인해 녹색 저감과 투명도 증가를 관찰하였다 (Fig. 2 (b), (c)). 이후 지속적으로 시료를 관찰한 결과, 모든 실험군에서 재성장이 확인되었으며 T_B > T_C > T_D > T_E > T_F > T_G 순으로 재성장이 빠르게 관찰되었다 (Fig. 2 (d), (e), (f)). 또한, 재성장시 초음파 조사시간이 2시간 이상인 실험군 (T_E, T_F, T_G) 대비 2시간 미만인 실험군 (T_B, T_C, T_D)은 시간 경과에 따라 육안상 더욱 진한 녹색을 띄는 것을 관찰하였다. 따라서 초음파 조사시간별 시료의 육안상 변화를 관찰한 결과, 2시간 이상 초음파 조사가 이루어져야 장기적인 조류 성장억제가 이루어질 것으로 판단된다.
3.2 Chlorophyll-a와 M. aeruginosa의 개체수 변화
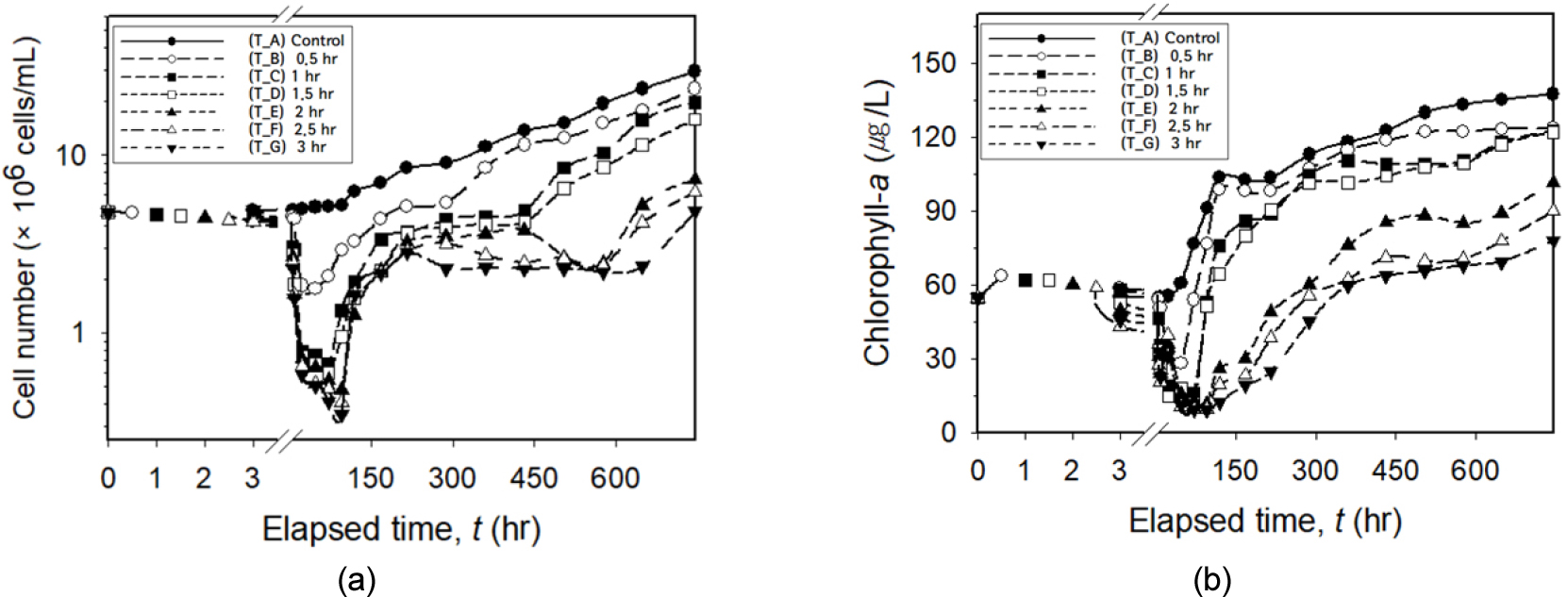
시간 경과에 따른 Chl-a와 M. aeruginosa의 개체수 변화를 관찰한 결과 (Fig. 3), 대조군은 관찰기간 동안 Chl-a 농도와 개체수의 지속적인 증가가 관찰되어 조류 성장억제 요인은 없는 것으로 판단된다. 모든 실험군에서는 초음파 조사 종료 이후 Chl-a 농도와 개체수의 저감이 관찰되었으나, 개체수 대비 Chl-a 값이 상대적으로 높음을 확인하였다. 이는 다른 연구 (KICT 1997)에서도 보고된 바가 있으며, 사멸하거나 부력조절 능력을 상실한 개체에서도 Chl-a가 일부 검출되어 개체수 대비 Chl-a 값이 상대적으로 높은 것으로 사료되며, 정확한 측정을 위해 본 연구는 개체수 기반으로 M. aeruginosa의 성장억제 평가를 진행하였다.
M. aeruginosa의 개체수 변화를 관찰한 결과 (Fig. 3 (a)), 초음파 조사시간이 2시간 미만인 실험군 (T_B, T_C, T_D)은 저감 이후 조류의 급격한 재성장이 관측되었다. 반면, 초음파 조사시간이 2시간 이상인 실험군 (T_E, T_F, T_G)은 2시간 미만 조사한 실험군 대비 조류성장억제가 약 1 - 2일 더 지속되는 것을 확인하였다. 또한 조류의 개체수가 초기 개체수로 회복되기까지 소요된 시간을 검토한 결과, 조사시간 2시간을 기준으로 실험군 T_B (0.5 hr)는 7일, T_C (1 hr)와 T_D (1.5 hr)는 약 20일, T_E, T_F, T_G ( t ≥ 2 hr)는 약 30일이 소요되어 초기 개체수까지 회복 시간의 차이를 확인하였다 (Table 1). 각 실험군의 최대 조류 성장억제 효율을 도출한 결과, 조사시간이 가장 높은 T_G (3 hr)의 제거율이 93%로 가장 높은 성장억제 효율이 도출되었으며, 조사시간이 증가할수록 성장억제 효율이 높아지는 것을 확인하였다 (Table 1). 따라서 종합적으로 검토하였을 때 조류 성장억제 기간과 초기 개체수까지 회복 시간은 초음파 조사시간과 비례하며, 정체수역 내 장기적 조류 성장억제를 위해서는 2시간 이상 초음파 조사가 필요한 것으로 조사되었다. Sim et al. (2006), Rajasekhar et al. (2012) 등의 선행연구에서도 초음파 조사시간에 비례하여 조류 성장억제 효율이 증가한다는 유사한 연구 결과가 도출되었으나, 단기간 (20 min)의 초음파 조사 시에도 즉각적인 조류 성장억제가 관찰되었다. 이는 본 연구 대비 고출력 (30 W L-1) 혹은 적은 시료량 (<500 mL)으로 실험이 진행되었기 때문에 단위부피당 초음파 에너지 (Watt L-1)가 높으며, 적은 용량의 시료 내 높은 밀도의 조류 개체수에서 초음파의 영향을 받는 조류의 개체수가 훨씬 많기 때문인 것으로 판단된다.
Table 1.
Summary of growth inhibition period, recovery time to initial concentration, and cell reduction under the various ultrasonic irradiation time
3.3 성장률과 일차분해율 분석
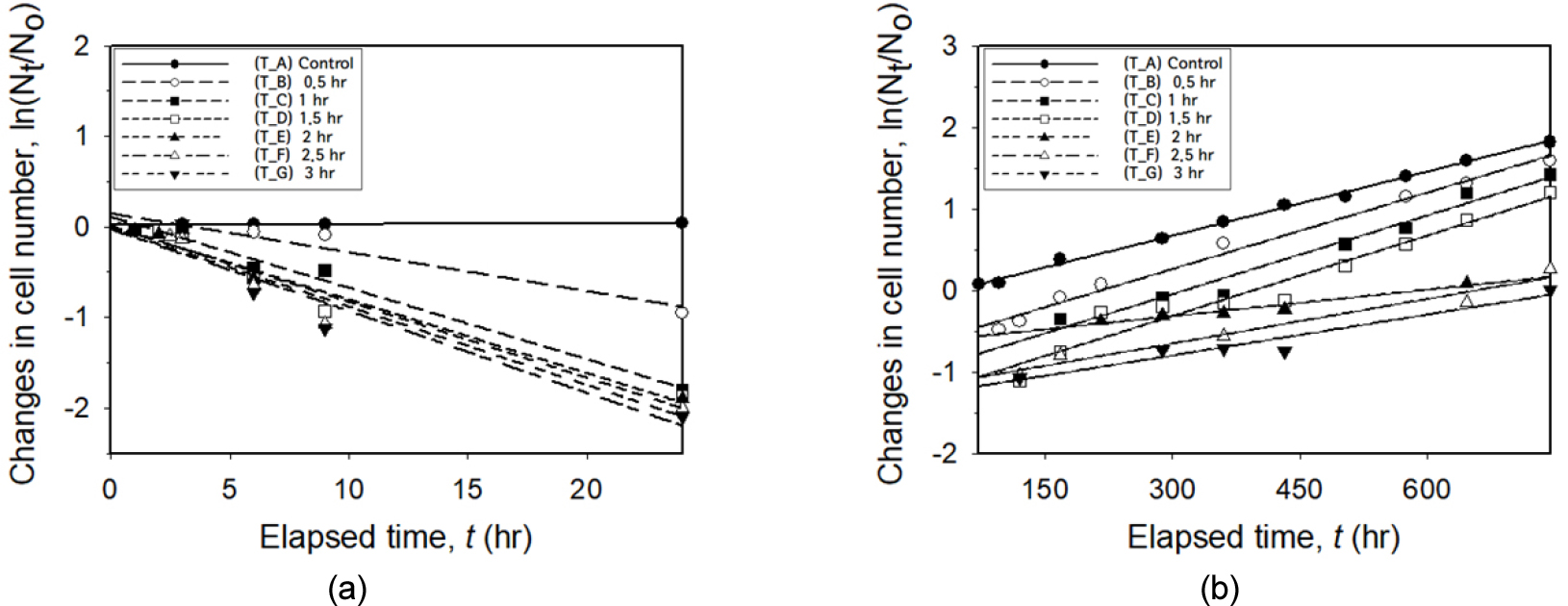
M. aeruginosa 개체수 변화를 통해 비성장속도 (μ)와 일차분해속도 (κ)를 도출한 결과 (Table 2, Fig. 4), 관찰기간 동안 대조군은 비성장속도가 0.7 × 10-3 - 2.6 × 10-3 hr-1로 조류의 성장이 확인되어 조류 성장억제 요인은 없는 것으로 판단된다. 실험군은 각각의 조류 성장억제 기간 동안 (T_B: t < 2 day, T_C, D: t < 3 day, T_E, F, G: t < 4 day) 성장률 대비 높은 일차분해속도 (κT_B = 43.0 × 10-3 hr-1, κT_C = 78.8 × 10-3 hr-1, κT_D = 81.3 × 10-3 hr-1, κT_E = 83.8 × 10-3 hr-1, κT_F = 86.5 × 10-3 hr-1, κT_G = 90.5 × 10-3 hr-1)가 도출되었으며, 초음파 조사시간과 비례하여 높은 일차분해율이 확인되었다. 이러한 결과는 선행연구 Jang et al. (2022)에서도 동일하게 실험군에서 성장률 대비 높은 일차분해속도 (κ)가 도출되었으나, 본 연구에서는 선행연구 (4.9 × 10-3 hr-1 – 13.0 × 10-3 hr-1) 대비 높은 일차분해속도가 도출되었다. 이는 Jang et al. (2022)에서 도출된 최적화된 주파수 (23 kHz) 및 출력 (6.94 W L-1)을 활용하여 실험을 진행함에 따라 조류가 효과적으로 빠르게 억제되어 높은 일차분해속도가 도출된 것으로 판단되나, 최적 초음파 조사에 따른 일차분해속도를 정확하게 도출하기 위해서는 추가적인 검증 실험이 요구된다.
Table 2.
Summary of specific growth rate (μ) and first order decay constant (k) of M. aeruginosa under the various ultrasound irradiation time
조류 성장억제 기간 이후 재성장 (μT_B = 3.1 × 10-3 hr-1, μT_C = 3.2 × 10-3 hr-1, μT_D = 3.3 × 10-3 hr-1, μT_E = 1.1 × 10-3 hr-1, μT_F = 1.8 × 10-3 hr-1, μT_G = 1.7 × 10-3 hr-1)이 관측되었으며, 초음파 조사시간이 2시간 미만인 실험군 (T_B, T_C, T_D) 대비 조사시간이 2시간 이상인 실험군 (T_E, T_F, T_G)의 경우 상대적으로 낮은 성장률을 보였다. 이는 장기간 초음파의 영향을 받은 M. aeruginosa는 충분한 에너지 전달로 인하여 기낭 등 내부기관과 세포막에 큰 손상을 받아 조류 성장억제 효과가 우수한 반면, 단기간 초음파의 영향을 받은 M. aeruginosa는 초음파 파장을 피해 침전되어 있거나 내부기관과 세포막 손상을 초래할 수 있는 임계에너지 이상의 충분한 에너지 전달이 이뤄지지 않아 재성장이 빠르게 일어나는 것으로 사료된다. 이러한 비성장속도와 일차분해속도의 변화를 근거로 조사시간이 길수록 조류 성장억제 기간과 재성장 주기가 증가되며, 본 연구조건에서 장기적인 조류 성장억제를 위해서는 최소한 2시간 이상 초음파 조사가 임계시간인 것으로 판단된다.
3.4 초음파에 의한 M. aeruginosa의 형태학적 변화
초음파 조사 전후의 M. aeruginosa의 형태학적 변화를 관찰하기 위하여 SEM과 TEM을 이용하여 세포 표면 및 내부 형질 변화를 비교 분석하였다. SEM 분석 결과, 대조군은 매끄러운 세포 표면 형태를 유지하며, 표면의 손상 (rupture)이 관찰되지 않았으나 (Fig. 5 (a)) 실험군 (T_E)은 세포 표면이 불규칙한 구형이며 초음파의 영향으로 인한 명확한 세포막의 손상이 관찰되었다 (Fig 5 (b)). 이는 선행 연구 결과 (Li et al. 2014, Li et al. 2019, Peng et al. 2020)와 동일하게 초음파의 공동현상으로 인하여 M. aeruginosa의 외부 세포막이 손상되어 세포 주변 환경과의 물질 교환 및 조절이 저해되고 생명 시스템 유지에 필요한 물질수송, 세포운동, ATP 생합성이 교란되어 성장억제로 이어지는 것으로 판단된다. TEM 분석 결과, SEM과 동일하게 초음파에 의한 조류 세포막의 손상으로 일부 세포막의 주름진 모습이 관찰되었다 (Fig. 6 (b)). 또한 실험군 (T_E)은 대조군 대비 M. aeruginosa 세포 내부 구조가 파괴된 것을 관찰하였으며. 조류 세포 내 기낭이 파괴되어 눈에 띄게 감소된 것을 확인하였다 (Fig. 6). 이러한 결과와 동일하게 Srisuksomwong et al. (2012), Kong et al. (2019), Park et al. (2019)에서도 초음파 조사로 인한 조류 세포 내 기낭의 감소를 관찰하여 보고한 바가 있다. 초음파에 의한 조류의 기낭 감소는 조류의 부력조절 능력을 상실시켜 조류를 침전시키고, 광합성작용을 차단함으로써 조류 성장을 억제를 초래한다. 그러나, 본 연구에서는 장기적인 관찰을 통해 Lee et al. (2000)에서 보고된 바와 같이 일정기간 경과 후 남조류 내 기낭의 재생으로 인한 조류의 재성장을 확인하였다. 따라서 정체수역에서 장기적 조류 성장억제를 위해서는 최소한 2시간 이상 초음파 조사를 주기적 간격을 두고 조사할 필요가 있으며, 이를 위해서는 정체수역 내 초음파 조사장치와 조류 모니터링 센서가 연계된 장치를 설치하여 일정농도 이상의 조류가 성장 시 임계에너지 이상의 초음파를 조사하여 유해남조류의 과도한 성장을 억제할 수 있을 것으로 판단된다.
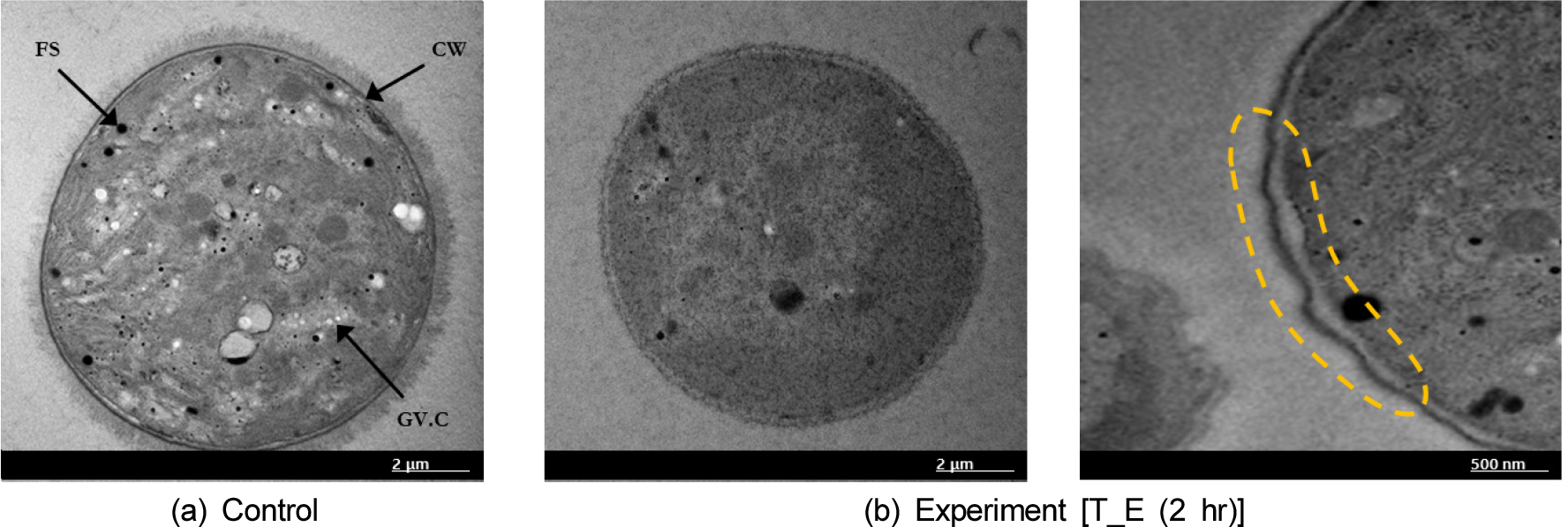
Fig. 6.
Transmission electron microscopy images of M. aeruginosa. (a) Control (normal cell) after 15 days, (b) 2 hr ultrasonic irradiation (note that dotted line indicates the damage of M. aeruginosa cell surface; FS indicates food storage particle; CW indicates cell wall; GV-C indicates gas vesicle in cross-section).
4. 결 론
본 연구는 수생태계의 위해성이 낮으며 유해남조류의 성장억제가 가능한 초음파 처리 방법을 이용하여 대용량 조류 시료를 대상으로 실험실 규모 실험을 진행하였으며 초음파 조사시간별 조류의 성장억제 효율 (efficiency)과 지속성 (sustainability)을 중점적으로 확인하였다.
초음파 적용 시간에 따른 육안상 변화를 관찰한 결과, 초음파 조사시간이 짧을수록 재성장이 빠르게 관찰되었으며, 재성장시 초음파 조사시간이 2시간 이상인 실험군 (T_E, T_F, T_G) 대비 2시간 미만인 실험군 (T_B, T_C, T_D)은 시간 경과에 따라 육안상 더욱 진한 녹색을 띄는 것을 관찰하였다.
M. aeruginosa 개체수 변화를 관찰한 결과, 초음파 조사시간이 2시간 미만인 실험군 (T_B, T_C, T_D)은 저감 이후 조류의 급격한 재성장이 관측되었다. 반면, 초음파 조사시간이 2시간 이상인 실험군 (T_E, T_F, T_G)은 2시간 미만 조사한 실험군 대비 조류성장억제가 약 1 - 2일 지속되는 것을 확인하였으며. 조사시간이 길수록 초기 개체수까지 회복 시간이 증가하는 것을 확인하였다.
비성장속도 (μ)와 일차분해속도 (κ)를 도출한 결과, 실험군은 조류 성장억제 기간 동안 성장률 대비 높은 일차분해속도가 도출되었으며, 초음파 조사시간과 비례하여 높은 일차분해율이 확인되었다. 재성장 기간 동안 초음파 조사시간이 2시간 미만인 실험군 (T_B, T_C, T_D) 대비 조사시간이 2시간 이상인 실험군 (T_E, T_F, T_G)의 성장률이 상대적으로 낮은 것을 확인하였다.
SEM, TEM 분석 결과, 실험군 (T_E)은 초음파의 영향으로 인한 M. aeruginosa의 세포 표면 및 세포막의 손상이 명확히 관측되었으며, 대조군 대비 실험군의 M. aeruginosa 세포 내 기낭이 파괴되어 감소된 것을 확인하였다.
종합적으로 검토하였을 때, 초음파에 의한 조류 성장억제 효과를 확인하였으며, 조류 성장억제 기간과 초기 개체수까지 회복 시간은 초음파 조사시간과 비례함을 확인하였다. 또한, 장기적인 조류 성장억제를 위해서는 최소한 2시간 이상 초음파 조사가 임계시간인 것으로 판단된다. 따라서 정체수역에서 장기적 조류 성장억제를 위해서는 최소한 2시간 이상 초음파 조사를 주기적 간격을 두고 조사할 필요가 있으며, 이를 위해서는 정체수역 내 초음파 조사장치와 조류 모니터링 센서가 연계된 장치를 설치하여 일정농도 이상의 조류가 성장 시 임계에너지 이상의 초음파를 조사하여 유해남조류의 과도한 성장을 억제할 수 있을 것으로 판단된다.