1. 서 론
2. 재료 및 방법
2.1 광미와 황철석
2.2 일광광산 토착세균 배양
2.3 연료전지 장치
3. 결과 및 고찰
3.1 광미를 활용한 전기 생산 가능성
3.2 황철석 함유량이 광미 활용 전기 생산에 미치는 영향
3.3 광미 활용 연료전지에서 토착세균의 역할
4. 결 론
1. 서 론
산성광산배수의 원인물질인 광물찌꺼기 (광미)는 선광 및 제련 과정 중 유용한 광물을 회수하고 남은 저품위 불용광으로 황철석을 포함한 황화광물을 포함하고 있다. 광미는 강수 및 공기와의 접촉으로 쉽게 산화반응이 일어나 산성광산배수 (acid mine drainage)를 발생시킨다. 산성광산배수는 황철석이 산화되어 발생한 황산이 포함되어 있기 때문에 낮은 pH를 가지며, 광미로부터 용출된 유해 중금속을 함유한다. 이러한 산성광산배수의 발생은 하천의 적화·백화 현상을 발생시키는 등 광산 주변의 수계와 토양 오염의 주요 원인이 되고 있다 (Johnson and Hallberg 2005, Ji et al. 2010, MRC 2013, KIGAM 2014a). 현재 우리나라의 현행 광산으로는 전남의 은산광산 (금, 은), 경북의 금호광산 (아연), 강원의 양양광산 (철), 신예미광산 (철), 충북의 광산 (몰리브덴)과 같은 금속광산이 있고, 채굴작업 후 선광작업에서 배출되는 광미는 광산에 적치되어 있는 실정이다 (KIGAM 2014b). 또한 폐광된 광산 중 다수의 석탄광산, 금속광산, 그리고 비금속광산에서 산성광산배수를 배출하여 폐광산 주변 환경에 영향을 주고 있다 (MRC 2013).
현재 광미의 처리 방법에는 매립법, 고형화/안정화법, 채굴적 충전법, 토양세척법, 무해화 등이 있지만, 처리 후 광미에 대한 별도의 용도가 없이 주로 적치 또는 매립되고 있다 (MRC 2014). 이러한 광미, 특히 황철석 성분을 함유한 광미가 지표환경에 노출되면 물과 산소에 의해 산화되어 Fe2+와 H+를 발생하고 (식 (1)), Fe2+는 Fe3+로 산화된다 (식 (2)). Fe3+는 Fe(OH)3로 침전되거나 (식 (3)), 그 자체가 산화제가 되어 황철석의 산화를 촉진한다 (식 (4)). 이 때, Fe2+의 산화반응은 (식 (2)) Acidithiobacillus ferrooxidans와 같은 철산화균에 의해 촉진될 수 있다 (Silverman and Lundgren 1958, Pesic and Oliver 1989, Leduc and Ferroni 1994, Baker and Banfield 2003, Gleisner et al. 2006, Ju et al. 2014). 단일균주에 의한 황철석의 산화보다 황을 산화시키는 박테리아가 포함된 혼합균주의 공생작용으로 인한 황철석의 산화가 더 촉진될 수 있다는 것이 확인되었다 (Bacelar-Nicolau and Johnson 1999).
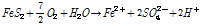 (1)
(1)
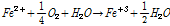 (2)
(2)
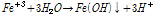 (3)
(3)
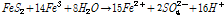 (4)
(4)
미생물연료전지는 화학전지에 미생물의 생물학적 반응을 적용하여 전기를 생산하는 방법으로, 음극부의 산화반응에서 생성된 전자가 양극부의 전극으로 이동하여 양극부에서 환원반응을 일으킨다 (Logan 2008). 이 때 음극부와 양극부 간에 발생하는 전위차가 전자의 흐름을 형성하여 전기를 생산할 수 있게 된다 (O’Hayre et al. 2006). 이러한 미생물연료전지에 광미와 철산화균을 적용하면, 철산화균에 의한 광미 내 황철석의 산화반응 촉진을 유도할 수 있다 (Silverman and Lundgren 1958, Pesic and Oliver 1989, Leduc and Ferroni 1994, Baker and Banfield 2003, Gleisner et al. 2006, Ju et al. 2014).
기존 연구에서는 광미에서 용출되어 나온 산성광산배수 내 철성분의 산화반응을 사용하여 전기를 발생한 바 있으나 (Cheng et al. 2007), 이는 이미 발생한 산성광산배수 처리에 초점을 두고 있어, 광미를 폐기물로 간주하여 자원으로 활용하지 않는다. 따라서 본 연구에서는 광미를 전기 생산용 자원으로 활용할 수 있는 가능성을 알아보고자 광미를 이용한 미생물연료전지를 구성하였고, 광미를 활용하여 전기를 생산할 때 광미 내 황철석 함량이 연료전지의 전기적 효율에 미치는 영향을 알아보았다. 또한, 광산 주변 토착미생물을 활용함으로써 광미를 이용한 미생물연료전지에서 미생물의 영향도 알아보았다. 광미 내 황철석 성분의 산화반응을 활용하면 전기 생산뿐 아니라 광미 내 산성광산배수 생성 우려물질을 제거하여 광미의 무해화 효과도 기대할 수 있다.
2. 재료 및 방법
2.1 광미와 황철석
본 연구에서는 황철석 성분이 함유된 광미를 사용하기 위해 Y 철광산 (pH 2.6, Eh 0.74 V)에서 습식 자력선광 후 배출된 광미를 사용하였다. 또한 광미 내 황철석 성분 함량의 영향을 알아보기 위해 페루 산 자연 황철석을 구입하여 사용하였다. 광미와 황철석의 조성은 XRF (Bruker AXS, Germany)를 사용하여 분석하였다 (Table 1). 황철석은 황철석 표면이 산소와 물과의 접촉이 최소가 되도록 주의하면서 막자사발을 이용하여 분쇄한 후 (<250 μm), 0.5 N HNO3로 세척하여 표면의 산화물을 제거하였다 (Bonnissel- Gissinger et al. 1998).
2.2 일광광산 토착세균 배양
본 연구에서 사용한 미생물은 일광 폐광산 갱구 부근 토양에서 분리한 토착세균을 사용하였다. 토양의 미생물 군집을 Pyrosequencing (Toche, Branford, CT, USA)을 통해 알아본 결과 Acidithiobacillus ferrivorans, Acidithiobacillus ferrooxidans, Leptospirillum ferroo-xidans 와 같은 철산화균이 있었다. 분리한 토착세균을 9K 배양액 (Silverman and Lundgren 1958)에 접종한 후 호기 조건에서 한 달 간격으로 계대 배양하였다 (30oC, 180 rpm). 9K 배양액의 조성은 다음과 같다 - (NH4)2SO4 3.0 g L-1, KCl 0.10 g L-1, K2HPO4 0.50 g L-1, MgSO4·7H2O 0.50 g L-1, Ca(NO3) 20.01 g L-1, FeSO4·7H2O 44.22 g L-1, 10 N H2SO4 1 mL L-1 (Silverman and Lundgren 1958). 지수기 (exponential phase)에 있는 미생물을 연료전지에 접종하기 위해 계대 배양한 후 modified-9K 배양액으로 세척하였다. Modified-9K 배양액은 기존 9K 배양액 (Silverman and Lundgren 1958)에서 FeSO4·7H2O를 생략한 배양액이다.
2.3 연료전지 장치
연료전지는 air-cathode와 single-chamber (5 x 5 x 5 cm3)의 음극부 (anode)를 가지도록 제작하였다. 광미 연료전지에는 광미를 modifed-9K 배양액 100 mL에 400 g L-1로, 황철석 연료전지에는 분쇄된 황철석을 modified-9K 배양액 100 mL에 100 g L-1로 넣은 후, 분리한 토착세균을 107 cells mL-1 이상이 되도록 접종하였다. 음극과 양극으로는 carbon cloth (0.35 mm, Ballard, USA), Nafion 117 (Dupont, USA), Pt-coated carbon cloth (0.5 mg-Pt cm-2, 20 wt% wet proof, Ballard, USA)를 140oC, 20 mPa로 3분간 압착한 MEA (membrane electrode assembly)를 사용하였다. 음극부에서는 황철석 또는 광미로부터 녹아 나온 Fe2+가 산화 (식 (5))되도록, 양극부의 Pt-coated carbon cloth에서는 대기 중의 산소가 환원 (식 (6))되도록 연료전지를 구성하였다. 연료전지의 전기적 특성을 확인하기 위하여 생성되는 전압을 20분 간격으로 multimeter (Kiethley 2700, USA)로 측정하였다. 개로전압이 안정화된 후, 음극과 양극을 10 kΩ로 연결하였다. 음극부의 산화반응과 양극부의 환원반응에 의해 생성된 전압 (V), 전류 (I), 외부저항 (Rext), 전력 (P)의 관계는 식 (7-8)을 이용하여 도출하였다. 도출된 전류와 전력값을 음극의 면적으로 나누어 전류밀도와 전력밀도를 계산하였다. 연료전지는 음극부 내 들어간 총 황철석 양을 기준으로 총 세 가지 조건으로 실온 (23oC)에서 운전하였다 (Table 2). 토착세균의 영향을 알아보기 위해 미생물을 접종하지 않은 조건에서도 운전하였다.
3. 결과 및 고찰
3.1 광미를 활용한 전기 생산 가능성
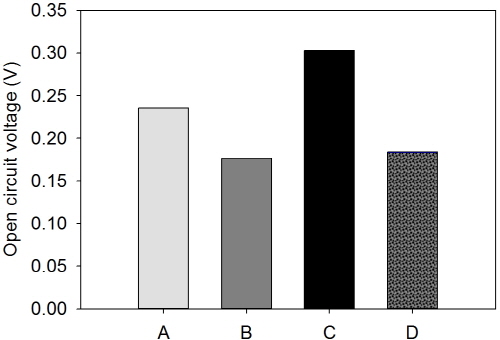
Fig. 1은 광미를 활용한 미생물연료전지의 개로전압을 보여준다. 개로전압이란 회로가 열린 상태에서 음극의 광미 산화반응과 양극의 산소 환원반응의 전위 차이이며, 이 값이 양수일 때에 연료전지가 성립할 수 있다 (O’Hayre et al. 2006). 토착세균이 있는 상태에서 음극 내 황철석 함량이 적은 (0.4%, 20.4%) 경우, 즉 광미만 있는 경우 (A)와 광미와 황철석이 섞여 있는 경우 (B) 개로전압이 각각 0.24 V와 0.18 V였으나, 황철석 함량이 100%로 증가하면서 (C) 개로전압도 0.30 V로 증가함을 볼 수 있다 (Fig. 1). 또한, 개로전압은 토착세균의 존재 유무에 크게 영향 받지 않았다 (Fig. 1). 이러한 양의 값을 가진 개로전압은 광미를 활용한 연료전지의 성립이 가능함을 보여준다.
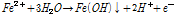 (5)
(5)
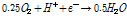 (6)
(6)
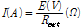 (7)
(7)
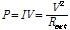 (8)
(8)
3.2 황철석 함유량이 광미 활용 전기 생산에 미치는 영향
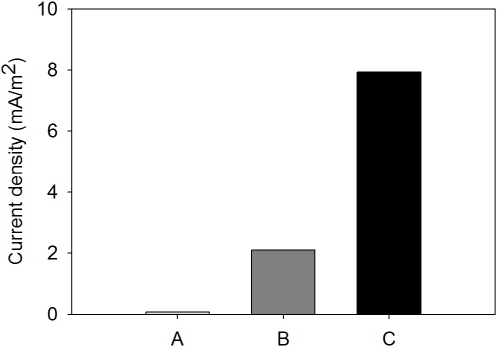
Fig. 2는 외부저항 (10 kΩ)과 연결된 미생물연료전지에서 황철석 함량이 연료전지 효율에 미치는 영향을 보여준다. 음극과 양극을 외부저항 (10 kΩ)과 연결한 후 발생하는 전기적 효율이 음극부 내 황철석 함량의 증가에 따라 증가하는 경향을 보였다 (Fig. 2). 황철석 함량이 0.4%에서 100%로 증가하면서 전류밀도도 0.076 mA m-2에서 7.9 mA m-2로 약 100배 정도 증가하였다 (Fig. 2). 마찬가지로, 전력밀도도 0.0001 mW m-2에서 1.5782 mW m-2로 증가하였다. 이는 음극부 내 황철석 함량이 높아짐에 따라 용출되어 나오는 초기 Fe2+ 양이 많아지고, 그래서 Fe2+ 산화 반응에 따른 전자 생산이 늘어나기 때문이라고 볼 수 있다 (Pesic and Oliver 1988, Rodriguez 2003). 마찬가지로, 광물 내 철의 함량이 높을수록 용존 Fe3+ 양이 많았고 (Rodriguez 2003), 이는 철의 함량이 높을수록 산화될 수 있는 초기 용존 Fe2+의 양이 많아지기 때문이다 (Pesic and Oliver 1988). 따라서 황철석 함량이 높을수록 전기적 효율이 높았다고 할 수 있다.
3.3 광미 활용 연료전지에서 토착세균의 역할
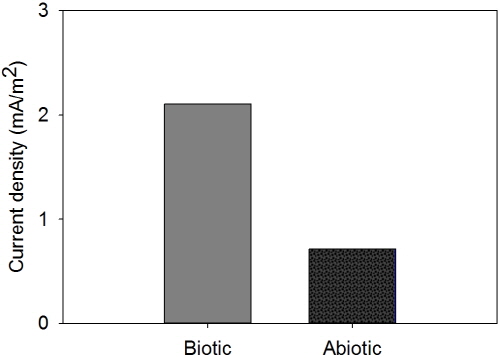
Fig. 3는 광미를 이용한 연료전지에서 토착세균 주입이 전류밀도에 미치는 영향을 보여준다. 토착세균의 주입은 전류밀도를 0.71 mA m-2에서 2.1 mA m-2로 약 세 배 정도 증가시켰고, 전력밀도 또한 0.013 mW m-2에서 0.11 mW m-2로 대략 10배 정도 증가시켜, 전기적 효율을 향상시켰다 (Fig. 3). 철의 산화환원반응에서 미생물의 대사는 중요한 역할을 하고 (Weber et al. 2006), 특히 철산화균은 황철석의 산화반응을 촉진한다 (Evangelou 1995, Baker and Banfield 2003). 따라서, 광미를 활용한 연료전지 운전은 미생물이 없을 경우도 가능하지만, 철산화에 관여하는 미생물 주입으로 전기적 효율을 높일 수 있다. 이는 철산화균이 황철석 산화과정중의 율속과정인 식 (2)에서의 Fe2+를 Fe3+로 산화를 촉진시켰기 때문인 것으로 추정한다. 또한, 본 연구에서와 같이 토착세균을 활용할 경우, 단일균주가 아닌 철산화에 관여할 수 있는 혼합균주를 사용하게 되어 철산화 반응을 더 촉진시킬 수 있다 (Bacelar-Nicolau and Johnson 1999).
4. 결 론
본 연구를 통해 광미에 연료전지 기술을 적용하여 전기 생산용 자원으로 활용할 수 있음을 확인하였다. 광미를 활용할 때, 광미 내 산화환원반응에 참여하여 전자를 생성할 수 있는 황철석과 같은 성분의 함량이 높을수록 연료전지의 효율이 향상되었다. 또한, 물이나 공기 노출에 의한 산화에 비해 철산화 능력이 있는 미생물을 주입하여 전기적 효율을 더 향상시킬 수 있다. 연료전지의 운전은 광미 내 중금속을 제거할 수 있을 것으로 예상되므로, 오염유발우려 물질의 처리 및 폐기물의 자원화를 도모할 수 있는 기술로 사용될 수 있을 것을 판단된다.