1. 서 론
2. 연구 방법
2.1 연구 지역 및 실험방법
2.2 서식지 면적 측정
2.3 부화율 측정
2.4 개체의 길이 측정
2.5 개구리의 발생 정도 측정
2.6 아성체 개체 길이 측정
2.7 데이터 처리
3. 결 과
3.1 서식지 면적 변화
3.2 실험구별 평균대기습도
3.3 실험구별 평균기온
3.4 실험구별 평균수온
3.5 부화율 결과
3.6 실험구별 유생 개체의 길이
3.7 고도별 개구리의 발생
3.8 실험구별 아성체 개체의 길이
4. 고 찰
1. 서 론
지구 온난화로 인해 지구 평균 기온은 지난 90년 동안 약 0.6°C 증가였으며 빠른 속도로 1°C까지 계속 증가 할 전망이다 (Root et al. 2003). 연간 지구 온도는 지난 20~25년간 크게 증가하고 있으며 전 세계적으로 많은 양서류 종이 계속 감소하고 있고 몇몇은 멸종하고 있다 (Blaustein and Wake 1990, 1995; Blaustein et al. 1994; Carey and Alexander 2003, Collins and Storfer 2003, Houlahan et al. 2000, Kiesecker et al. 2001, La Marca et al. 2005, Laurance 1996, Lips 1998, Pounds 2001, Pounds and Crump 1994, Stuart et al. 2004). 최근 발생하고 있는 지구온난화는 기온, 강수량, 일조량 등에 따라서 결정되는 양서류의 번식지 출현 시기에 영향을 미칠 것으로 예상된다 (Heo et al. 2013). 이러한 환경의 변화는 양서류 서식지를 파괴시키며 (Saunders et al. 1987, Marsh and Pearman 1997, Lindenmayer et al. 1999), 양서류군집의 안정성을 감소시킨다 (Pausas et al. 1995, Pearman 1997). 지난 반세기 동안 세계 도처에서 진행되고 있는 환경오염 및 서식지의 감소는 양서류 다양성의 감소를 초래하였고 이는 먹이 연쇄의 구조와 기능을 변화시켜 생태계의 교란요인으로 부각되었다 (Cogger and Zweifel 1998).
양서류는 생태계 구성에 있어서 먹이사슬의 중간단계에 있으며, 생태계의 안정성을 위해 매우 중요한 분류군으로, 육상 및 수서 곤충을 포식하며 생활하고 파충류, 포유류, 조류의 주요 먹이원이 된다 (Song et al. 2009). 양서류 유생은 수중생태계의 1차 소비자이자, 상위 포식자의 중요한 먹이 자원이며, 성체는 육상과 수생생태계의 먹이사슬을 연결시켜주는 역할을 담당한다. 또한 양서류는 피부호흡을 하고 유생에서 성체로 변태하는 시기에 취약하며, 산란된 알이 외부환경에 직접 노출되어 있기 때문에 환경변화에 민감한 반응을 보인다. 따라서 양서류는 환경변화를 감지하고 (Lips et al. 2001) 습지생태계 건강성을 평가할 수 있는 효과적인 생물 지표로 널리 인식되고 있다 (Wyman 1990).
야생동물의 서식지는 여러 유형의 환경 요소로 이루어져 있으며 종의 분포와 서식지 이용 패턴은 각 종이 선호하는 자원의 이용 방식에 따라 달라진다 (Li et al. 1997). 한국산개구리의 산란분포는 고도 200 m이하에서 주로 이루어지고 있으며, 계곡산개구리의 경우, 200 m에서 1,000 m까지 이루어지고 있다. 따라서 양서류의 서식지의 산란특성을 파악하는 것은 향후 기후변화에 대한 생물모니터링에 있어서도 중요한 사항이 될 수 있다 (Gye 2003). 또한 산림의 수직적 구조와 환경 요소가 개체군의 분포에 미치는 영향과 이들 간의 상호작용을 이해하는 것은 야생동물의 분포를 예측하고 보전하는데 있어서 중요하다고 할 수 있다 (Ji and Jeske 2000).
이에 본 연구는 양서류 중 척삭동물문 양서강 무미목 개구리과에 속해있는 계곡산개구리 (Huanren brown frog, Rana huanrensis)를 통하여 자연 서식지에서의 계곡산개구리 알의 부화율, 개체의 길이, 아성체 개체의 길이, 평균 대기습도, 기온, 수온을 알아보고자 하였으며 이에 다음과 같은 가설을 설정하여 연구를 진행하였다. 서식지의 면적이 넓을수록 개체의 길이가 길어질 것이다. 서식지의 면적이 넓을수록 개체의 변태기간이 줄어들 것이다. 또한, 부화율이 82.6% 이하일 것이다. 이때 부화율의 설정은 Na et al. (2015) 연구를 참조하였다.
서식지의 면적에 따른 계곡산개구리의 생장률에 대한 본 연구는 향후 지구온난화에 따른 서식지의 면적 감소가 계곡산개구리에 미치는 영향을 이해하는데 도움을 줄 것으로 기대된다.
2. 연구 방법
2.1 연구 지역 및 실험방법
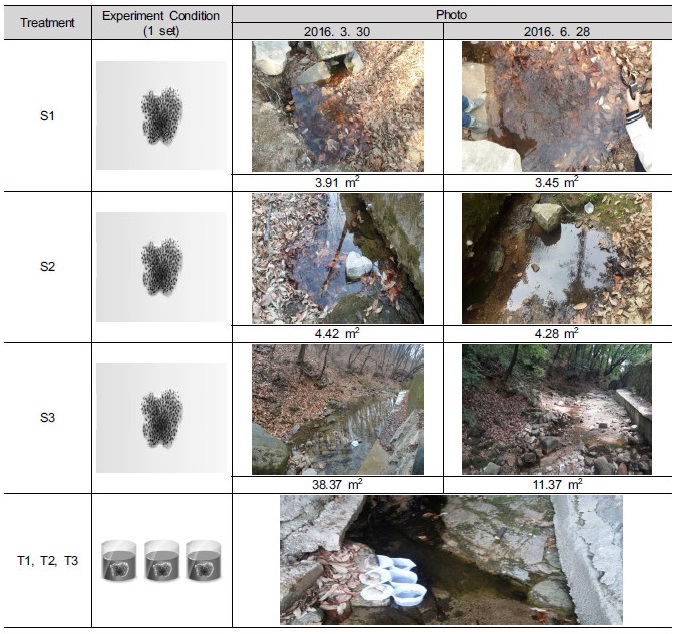
본 연구는 2016년 3월 30일 서울 노원구 상계동 수락산 일대 (37°40'55.86"N, 127°05'19.99"E)에 서식하는 계곡산개구리 (Rana huarenensis)를 이용해 진행하였다. 수락산 일대 계곡을 계곡산개구리 서식지 면적의 크기에 따라 가장 좁은 면적의S1 (37°41'00.4"N, 127° 05'16.2"E; 150 m), 중간 면적의 S2 (37°40'59.4"N, 127° 05'14.8"E; 120 m), 가장 넓은 면적의S3 (37°40'55.5"N, 127°05'21.1"E; 90 m)로 3개의 조사지역으로 나눈 후 각 조사지역 마다 주 2회 15개체를 무작위로 포획하여 개체의 발생정도와 개체의 길이를 측정하였으며, 수온계와 온습도계측정기를 이용하여 습도, 기온, 수온을 확인하였다. 부화율은 S2 지점에서 세 개의 난괴를 지정하여 측정 하였으며, 3개의 난괴는 각각 T1, T2, T3으로 명명하였다 (Table 1).
2.2 서식지 면적 측정
서식지 면적 측정은 2016년 3월 30일과 2016년 6월 28일 총 2회 시행하였다. 계곡을 가로질러 사선으로 가장 긴 부분과 짧은 부분을 측정하여 면적을 구하였다. 이때 측정 방법은 1회와 2회 동일하게 측정하였다.
2.3 부화율 측정
실험군 S2 의 난괴 중 3개 (T1, T2, T3)를 실험 대상으로 지정하여 주 2회 개체의 발생 정도와 부화율을 확인하였다. 개체가 부화할 때마다 개체수를 세며, 이때 부화한 개체는 난괴를 완전히 빠져 나와 스스로 헤엄을 치고 있는 개체만을 기록하였다. 난괴 안을 빠져 나오지 못하고 죽은 개체는 폐사한 개체로 기록하였으며, 위와 같은 방법으로 난괴에서 모든 개체가 부화할 때까지 측정하였다.
2.4 개체의 길이 측정
각각의 실험군 S1, S2, S3는 주 2회 수온과 대기온도, 대기습도, 발달정도, 개체의 길이가 측정되었다. 측정대상은 각 실험구 내 무작위로 포획된 15개체로 지정하였으며, 개체의 길이는 머리의 끝부터 꼬리의 끝을 기준 (SVL: Snout-vent length)으로 측정되었다.
2.5 개구리의 발생 정도 측정
각 실험군의 개체 성장 정도를 주 2회 측정하였다. 발생정도는 3단계 즉 뒷다리 발생, 앞다리 발생, 꼬리 퇴화로 나누어 기록하였으며, 측정대상은 각 실험구 내 무작위로 포획된 15개체 중 뒷다리가 발생된 된 개체로 지정하였다. 뒷다리 측정과 앞다리 측정은 1 mm 이상 발생하였을 때 기록하고, 꼬리 퇴화는 개체의 꼬리가 완전히 사라졌을 때 기록하였다.
2.6 아성체 개체 길이 측정
실험군 S1, S2, S3는 아성체의 길이를 비교하기 위해 각각의 실험구에서 무작위로 포획된 15개체들 중 아성체를 달성한 개체를 측정하였다. 아성체 길이 측정은 뒷다리와 앞다리가 발생하고 나오고 꼬리가 완전히 사라졌을 때 기록하였다.
2.7 데이터 처리
실험군 S1, S2, S3에서 주 2회 개체의 발생정도, 개체의 길이를 주 2회 조사하였다. 기온과 습도, 수온을 측정하고 측정 기록을 평균 내어 각 실험구의 평균값을 구하였으며, 개체 길이와 발생정도는 통계 프로그램을 통해 실험구별 평균과 오차를 계산하였다. 마지막으로 실험구별 평균값이 서로 유의하게 차이가 있는지 검증하기 위하여 F-test를 실행하였다.
3. 결 과
3.1 서식지 면적 변화
실험구별 서식지의 면적을 측정한 결과, 실험시작일인 2016년 3월 30일의 서식지 면적은 S1은3.91 m2, S2 는4.42 m2, S3 는 38.37 m2 로 측정되었으나, 실험 종료일인 2016년 6월 28일의 서식지 면적은 S1는3.45 m2, S2 는4.28 m2, S3 는 11.37 m2 로 줄어들었다 (Table 1).
3.2 실험구별 평균대기습도
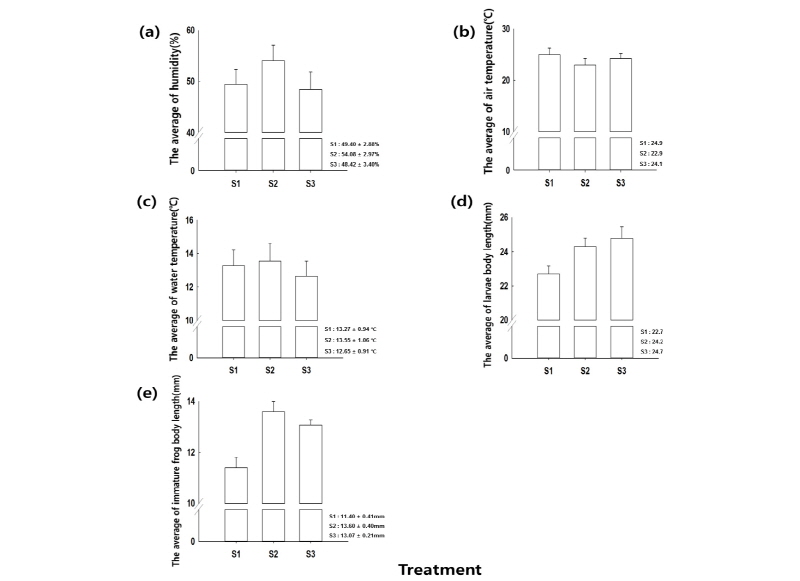
실험구별 평균대기습도를 측정 한 결과, S1의 평균대기습도는 49.40 ± 2.88%, S2는 54.08 ± 2.97%, S3는 48.42 ± 3.40% 로 측정되었다 (Fig. 1 a).
3.3 실험구별 평균기온
실험구별 평균기온을 측정 한 결과, S1의 평균대기온도는 24.99 ± 1.26°C, S2는 22.98 ± 1.22°C, S3는 24.19 ± 0.99°C로 측정되었다 (Fig. 1 b).
3.4 실험구별 평균수온
실험구별 평균수온을 측정 한 결과, S1의 평균수온은 13.27 ± 0.94°C, S2 은 13.55 ± 1.06°C, S3는 12.65 ± 0.91°C로 측정되었다 (Fig. 1 c).
3.5 부화율 결과
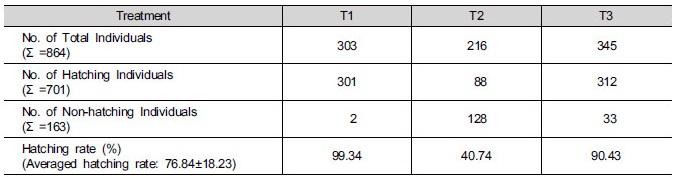
난괴의 부화율을 각각 측정한 결과, T1은 총 303개의 개체 중 301개체가 부화하여 99.34%, T2는 총 216개의 개체 중 88개체가 부화하여 40.74%, T3는 총 345
개의 개체 중 312개체가 부화하여 90.34% 의 부화율로 측정되었다. 그 결과 계곡산개구리의 최종 평균 부화율은 76.84 ± 18.23%으로 확인되었다 (Table 2).
Table 2. The Huanren brown frogs’ hatching rate on each treatment. Hatching rate was determined in S2, three egg’s
sacs were respectively named T1, T2, T3.
 |
3.6 실험구별 유생 개체의 길이
실험구별 계곡산개구리 유생 개체의 길이를 측정 한 결과, S1의 개체의 평균 길이는 22.71 ± 0.45 mm, S2는 24.29 ± 0.50 mm, S3는 24.77 ± 0.68 mm로 측정되었다. 위 결과에 대해 F-test를 한 결과, 실험구별 개체의 길이는 통계적으로 차이가 나타났다 (F-test p< 0.05, Fig. 1 d).
3.7 고도별 개구리의 발생
3.7.1 뒷다리 발생
연구 시작 일로부터 첫 뒷다리 발생 개체를 발견한 기간은 S1, S2, S3의 모든 실험구가 74일로 측정되었으며, 평균 개체의 길이는 각각 S1은 30.58 ± 0.05 mm, S2은 34.13 ± 0.05 mm, S3는 35.80 ± 0.06 mm로 측정되었다.
3.7.2 앞다리 발생
연구 시작 일로부터 첫 앞다리 발생 개체를 발견한 기간은 S1은 90일, S2은 74일, S3는 74일로 측정되었으며, 평균 개체의 길이는 각각 S1은 33 mm, S2는 32 mm, S3 는 34.25 ± 0.17 mm로 측정되었다.
3.7.3 꼬리 퇴화
연구 시작일로부터 첫 꼬리 퇴화 개체를 발견한 기간은 S1은 90일, S2는 83일, S3는 83일로 측정되었다.
3.8 실험구별 아성체 개체의 길이
실험구별 계곡산개구리 개체의 길이를 측정 한 결과, S1의 개체의 평균 길이는 11.40 ± 0.41 mm, S2는 13.60 ± 0.40 mm, S3는 13.07 ± 0.21 mm로 측정되었다. 위 결과에 대해 F-test를 한 결과, 실험구별 개체의 길이는 통계적으로 차이가 나타났다 (F-test p< 0.05, Fig. 1 e).
4. 고 찰
야생동물의 서식지는 여러 유형의 환경 요소로 이루어져 있으며 종의 분포와 서식지 이용 패턴은 각 종이 선호하는 자원의 이용 방식에 따라 달라진다 (Li et al. 1997). 따라서 양서류의 서식지의 산란특성을 파악하는 것은 향후 기후변화에 대한 생물모니터링에 있어서도 중요한 사항이 될 수 있다 (Gye, 2003). 이에 본 연구는 자연 서식지에서의 계곡산개구리의 생장률을 알아보기 위해 진행되었다.
실험구별 서식지의 면적을 측정한 결과, 실험시작일인 2016년 3월 30일과 실험 종료일인 2016년 6월 28일 사이에 모든 실험구의 서식지 면적이 감소하였다. S1은 3.91m2에서 3.45 m2로 감소하였으며, S2는 4.42 m2 에서 4.28 m2로 감소하였고, S3는 38.37 m2에서 11.37 m2 로 감소하였다. 이 결과 S3지점이 가장 큰 폭으로 서식지 면적이 줄어들었음을 확인할 수 있었다.
실험구별 평균대기습도는 S1에서 49.40 ± 2.88%, S2에서 54.08 ± 2.97%, S3에서 48.42 ± 3.40%으로 측정되었고, 실험구별 평균기온은 S1에서 24.99 ± 1.26°C, S2에서 22.98 ± 1.22°C, S3에서 24.19 ± 0.99°C으로 측정되었으며, 실험구별 평균수온은 S1에서 13.27 ± 0.94°C, S2에서 13.55 ± 1.06°C, S3에서 12.65 ± 0.91°C로 측정되었으나 F-test결과 세 가지 요소는 통계적으로 유의한 차이가 없었다.
계곡산개구리의 평균부화율을 분석한 결과, T1은 99.34%, T2는 40.74%, T3는 90.34%의 부화율로 나타났으며 계곡산개구리의 최종 평균 부화율은 76.84 ± 18.23%으로 측정되었다.
실험구별 유생 개체의 평균 길이를 분석한 결과, S1은 22.71 ± 0.45 mm, S2은 24.29 ± 0.50 mm, S3는 24.77 ± 0.68 mm로 측정되었으며, F-test결과 유의함으로 나타났다. 위의 결과로 보아 서식지의 면적이 넓을수록 개체의 길이가 늘어남을 확인 할 수 있었다.
연구 시작 일로부터, 첫 뒷다리 발생 개체를 발견한 기간은 S1, S2, S3의 모든 실험구가 74일로 측정되었으며 첫 앞다리 발생 개체를 발견한 기간은 S1은 90일, S2은 74일, S3는 74일로 측정되었고 첫 꼬리 퇴화 개체를 발견한 기간은 S1은 90일, S2은 83일, S3는 83일로 측정되었다. 이 결과 서식지의 면적이 넓을수록 개체의 변태기간이 짧아짐을 입증하였다.
실험구별 아성체 개체의 평균 길이를 분석한 결과, S1은 11.40 ± 0.41 mm, S2은 13.60 ± 0.40 mm, S3는 13.07 ± 0.21 mm로 측정되었으며, F-test결과 유의함으로 나타났다. 그러나 앞서 명시한 실험구별 평균대기습도, 평균기온, 평균습도의 결과는 유의하지 않았기 때문에 개체의 길이의 차이가 세 요소는 무관한 것으로 판단되며, 따라서 이러한 차이에는 실험구별 서식지의 면적과 수량의 변화가 영향을 미쳤을 것으로 예상된다. Pearman (1993)에 따르면 서식지의 면적이 양서류 개체의 길이에 영향을 미칠 수 있음을 언급하였으며, Kim and Jung (2014)은 물이 마를 위험이 있는 서식지에서 사는 양서류는 물이 마를 위험이 없는 서식지에 사는 양서류 보다 SVL이 작게 나타남을 밝혔다. 세 실험구중 S3 실험구의 서식지 면적이 38.37 m2에서 11.37 m2로 가장 큰 폭으로 감소되었기 때문에 위와 같은 결과가 나타났을 것으로 판단된다.
본 연구와 인위적 환경을 조성한 Na et al. (2015)의 결과를 비교 분석해보았을 때 자연 상태 개체의 부화율 평균은 76.84 ± 18.23%이었으나 인위적 환경을 조성한 개체의 부화율 평균은 82.56 ± 0.81%로 자연 상태에서보다 높은 결과로 나타났다. 자연 상태 개체의 첫 뒷다리 발생기간 평균은 74일, 앞다리 발생기간 평균은 79.33일, 꼬리 퇴화 기간 평균은 85.33일이었으나 인위적 환경을 조성한 개체의 뒷다리 발생기간은 80일, 앞다리 발생기간은 88일, 꼬리 퇴화 기간은 91일로 자연 상태에서보다 긴 기간으로 측정되었다.
자연 상태 아성체 개체의 길이는 12.69 ± 0.24 mm (n=45)이였으나 인위적 환경을 조성한 아성체의 길이는 17.00 ± 0.00 (n=2)로 자연 상태의 결과와 비교해 보았을 때 유의미한 차이가 났다. 위의 결과를 분석해 보았을 때 인위적 환경에서의 개체는 자연 상태의 기후, 천적과 같은 외적인 스트레스가 차단되었기 때문에 개체의 성장에 긍정적인 영향을 미쳤다고 예상된다.
본 연구에서는 서식 면적에 따른 계곡산개구리의 생장률 차이에 집중하여 연구를 진행하였으나, Song and Lee (2009)에 따르면 양서류 종에 대한 전국분포 현황 및 서식현황에 대한 연구들은 각종 보고서나 논문 등을 통해 발표되고 있으나, 각 종에 대한 고도별 분포연구는 매우 빈약한 실정이라고 언급 하였으며, 또한 Gye (2003)는 양서류의 고도별 산란특성을 파악하는 것은 향후 기후변화에 대한 생물모니터링에 있어서도 중요한 사항이 될 수 있음을 주장하였다. 본 연구의 결과를 바탕으로 추후 고도의 차이가 계곡산개구리의 생장에 미치는 영향에 대한 실험을 진행한다면 계곡산개구리 개체군의 서식환경을 이해하는데 큰 도움을 줄 것으로 기대된다.