1. 서 론
2. 연구방법
2.1 재료
2.2 산・염기 화학사고 상황 모사
2.3 분석
3. 결 과
3.1 화학반응 이전 토양의 물리・화학적 특성
3.2 화학반응 이후 토양의 물리・화학적 특성 변화
3.2.1 토양 입도 분포 및 비표면적
3.2.2 유기물 함량
3.2.3 토양 pH
3.2.4 양이온교환능력 (CEC)
3.2.5 치환성 양이온
4. 고 찰
5. 결 론
1. 서 론
최근 각종 산업단지에서의 화학물질 누출, 폭발 및 화재 등으로 인한 화학사고 및 이로 인한 피해사례가 꾸준히 보고되고 있다. 2012년의 구미 산업단지에서 발생한 불산가스 누출 사고는 많은 인명피해를 유발하였다. 당시 사고로 인해 5명이 사망하고 18명이 부상을 입었으며 12,000여 명이 병원치료를 받았다 (Lee 2013). 또한 이로 인해 사고주변지역에서 재배하는 벼에서도 불소가 최대 9,594 mg/kg까지 검출되기도 하였다 (Lee 2014).
환경부 화학안전정보공유시스템에 등록된 2014년부터 현재까지의 화학사고 사례 303건 중 강산 (HCl, 황산, 불산, 질산, 과산화수소 등)이나 강염기 (암모니아, NaOH 등)에 의한 화학사고 사례는 144건으로 산・염기 물질에 의한 사고 비중은 약 48%로 매우 높다 (Ministry of Environment 2017). 강산이나 강염기 물질은 인체나 환경에 치명적인 영향을 미치는 급성유해성을 가지고 있다 (Agency for Toxic Substances and Disease Registry 2017, Korea Occupational Safety and Health Agency 2017). 이러한 급성 유해성 외에도, 강산이나 강염기 물질이 토양에 유입되면 pH 변화를 초래하며 점토광물이나 토양유기물 등 토양구성물질과 반응하여 토양의 물리・화학적 변화를 일으킨다. 이는 생물의 성장 등 생태학적 영향을 미치는 문제를 발생시킬 수 있다. 강산 물질이 토양에 유입되면 알루미늄이나 철 산화물이 용해되고, 용해된 알루미늄이나 철이 인산을 불용화하여 식물의 영양소로 사용되는 인산 농도를 감소시키는 문제, 용해된 알루미늄이 점토광물에 치환되어 식물의 영양소로 사용되는 알칼리성 양이온 (K+, Na+, Ca2+, Mg2+ 등)의 함량이 감소하는 문제, 토양수분 내에 이온의 농도가 식물독성이 발현될 수준으로 증가되는 문제 등이 발생할 수 있다. 또한 강산이 유입되면 토양유기물 중 fulvic acid가 용해될 수 있다 (Hillel and Hatfield 2005). 한편, 강염기가 토양에 유입되면 양이온 농도가 증가해 토양수분의 염분 및 전기전도도 농도가 높아져 식물독성이 발생하는 문제나 토양수분 내 독성이온 (B3+, Na+, Cl-, Li+) 농도가 증가하는 문제가 발생할 수 있다. 특히 나트륨 계열의 강염기가 유입되면 토양의 팽윤 능력이 증가하여 토양의 투수성이 감소되고 bicarbonate 농도 증가에 따른 독성 발현 문제 등이 발생할 수 있다. 또한, 강염기 물질이 토양에 유입되면 식물의 양분 역할을 하는 토양유기물 중 humic acid 및 fulvic acid가 용해될 수 있다 (Bohn et al. 2002).
국립환경과학원은 「화학물질 위해성평가의 구체적 방법 등에 관한 규정」에 따라서 환경매질 (수질, 토양, 퇴적물, 대기 등)에 존재하는 화학물질의 위해성평가를 실시한다 (National Institute of Environmental Research 2014). 이 지침은 화학물질의 급/만성 인체 및 환경유해성을 파악하며 이를 통하여 위해도를 측정하는 지침이다. 토양의 물리・화학적 변화에 따른 토양의 생태기능 변화는 강산이나 강염기 물질이 고유하게 가지고 있는 유해성이 아니기 때문에 「화학물질 위해성평가의 구체적 방법 등에 관한 규정」에 의해서는 평가되지 않는다. 따라서 강산이나 강염기로 인한 화학사고가 발생한 경우, 이들 물질의 고유한 유해성으로 인한 인체 및 환경영향 외에도 토양 특성 변화에 의해 유발될 수 있는 영향을 평가하는 방안도 마련되어야 한다. 본 연구에서는 이러한 영향평가 방안의 일환으로 강산이나 강염기 물질이 토양에 유입되었을 때 변할 수 있는 토양의 물리・화학적 특성의 유형을 우선적으로 파악하였다. 이를 위해 본 연구에서는 토양에 강산이나 강염기 물질을 다양한 농도로 주입하고, 농도에 따라 발생할 수 있는 토양의 물리・화학적 특성 변화를 관찰하였다. 본 연구에서 평가한 토양의 물리・화학적 특성은 토양의 입도 분포, 비표면적, 유기물 함량, pH, 양이온교환능력 (cation exchange capacity, 이하 CEC), 치환성 양이온 중 알칼리성 양이온 (Na+, Ca2+, Mg2+, K+) 및 알루미늄 (Al3+) 이온 함량이었다.
2. 연구방법
2.1 재료
본 연구에 사용된 토양은 서울대학교 부근 관악산에서 채취하였다. 채취한 토양을 2 mm로 체거름한 후 풍건하여 상온에 보관하였다. 본 연구에서는 개별 물질 별로 사고 빈도가 가장 높은 HCl과 NaOH를 강산 및 강염기 화학사고 물질로 선정하였다 (National Institute of Environmental Research 2013).
2.2 산・염기 화학사고 상황 모사
본 연구에서는 강산 및 강염기 물질이 유출되어 토양과 완전히 반응하여 자연 배수된 상황을 모사하고자 하였다. 화학사고 모사를 위하여 토양 50 g과 HCl 용액 (0.001, 0.01, 0.1, 1, 10 M) 혹은 NaOH 용액 (0.001, 0.01, 0.05, 0.1, 1 M) 250 mL를 500-mL high density polyethylene (HDPE) bottle에 넣고 30°C에서 30 rpm의 속도로 7일간 교반하였다. 예비 실험 결과 7일은 토양과 산 또는 염기가 충분히 반응하여 토양의 pH가 안정하게 유지되는데 충분한 시간이었다. 교반 후 자연 배수 상황을 모사하기 위해 HCl 혹은 NaOH과 반응한 토양의 수분함량을 1/3 bar로 진공 여과하여 포장용수량 (field capacity)으로 조절하였다 (Veihmeyer and Hendrickson 1949). 이 때 여과지로는 0.45 µm 필터 (Corning Bottletop Filter)를 사용하였다.
2.3 분석
본 연구에서는 HCl 혹은 NaOH와 화학반응이 일어나기 전후 토양의 물리・화학적 특성을 분석하여 비교하였고, 분석대상 항목은 토양의 입도 분포, 비표면적, 유기물 함량, 토양 pH, CEC, 치환성 양이온 중 Na+, Ca2+, Mg2+, K+ 및 Al3+ 함량이었다. 토양의 입도 분포는 pipette method로 분석하였으며 (Miller and Miller 1987), 토양의 비표면적은 질소흡착에 의한 Brunauer, Emmett and Teller (BET) method로 측정하였다 (Brunauer et al. 1938). 토양 pH를 측정하기 위하여 토양과 증류수를 고액비 1:5 비율로 하여 한 시간 동안 교반하였으며 30분 동안 정치시킨 후 상등액의 pH를 측정하였다 (Conyers and Davey 1988). 유기물 함량은 Walkley-Black method로 분석하였으며 (Walkley and Black 1934), CEC와 알칼리성 양이온의 함량은 모두 ammonium acetate method (Schollenberger and Simon 1945)로 측정하였다. CEC는 암모늄 이온을 Kjeldahl 증류하여 0.01 N H2SO4 용액으로 적정한 후 정량화 하였으며 단백질/질소 자동분석기 (Kjeltec auto 2400/ 8400 System Tecator AB, Sweden)를 사용하여 분석하였다. 알칼리성 양이온 함량에 대한 정량은 유도결합플라즈마발광광도기 (ICP-OES, iCAP 7400 DUO, Thermo Scienfitic, USA)를 이용하여 분석하였다. 치환성 양이온 중 알루미늄 이온은 1 M KCl 용액으로 추출하여 마찬가지로 ICP-OES로 분석하였다 (Lin and Coleman 1960).
3. 결 과
3.1 화학반응 이전 토양의 물리・화학적 특성
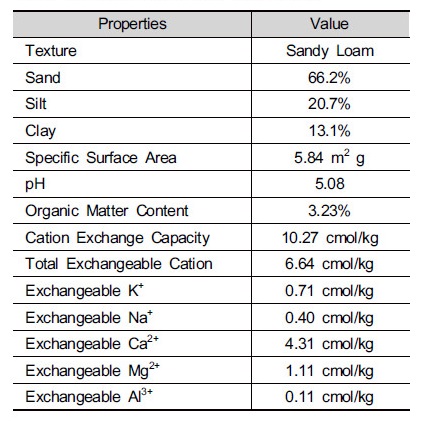
화학반응 이전 토양의 물리・화학적 특성은 Table 1에 정리되어 있다. 모래, 실트 및 점토의 비율은 각각 66.2, 20.7 및 13.1%로 sandy loam의 조성을 가졌으며 비표면적은 5.84 m2/g이었다. 또한 토양 pH는 5.08로 약산성 토양이며 유기물 함량은 3.23%였다. 양이온교환능력은 10.27 cmol/kg이며 알칼리성 양이온인 Na+, Ca2+, Mg2+, K+ 함량은 각각 총 치환성 양이온 6.64 cmol/kg의 6.1, 64.8, 16.7 및 10.7%인 0.40, 4.31, 1.11 및 0.71 cmol/kg였다. Al3+의 함량은 0.11 cmol/kg으로 총 치환성 양이온의 1.7%였다.
3.2 화학반응 이후 토양의 물리・화학적 특성 변화
3.2.1 토양 입도 분포 및 비표면적
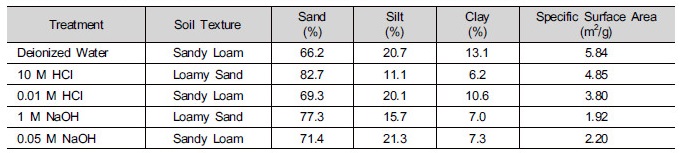
화학반응 이후의 토양 입도 분포와 비표면적은 Table 2와 같다. HCl이나 NaOH 농도가 각각 10 M이나 1 M인 경우 유의한 수준의 토양 입도 분포 및 비표면적 변화가 관찰되었다. 10 M HCl 혹은 1 M NaOH 용액과 반응한 토양의 모래의 함량이 기존 66.2%에서 각각 82.7, 77.3%로 늘어났으며 실트의 함량은 20.7%에서 11.1, 15.7%로, 점토의 함량은 13.1%에서 6.2, 7.0%로 감소하였다. 이로 인하여 화학반응 이전 토양의 토성은 sandy loam이었으나 10 M HCl 혹은 1 M NaOH과 반응한 후 모두 loamy sand로 토성이 변화하였다.
토양의 비표면적은 화학반응 전 5.84 m2/g에서 10 M HCl 용액과 반응시킨 경우 4.85 m2/g로, 1 M NaOH 용액과 반응시킨 경우 1.92 m2/g로 모두 감소하였다. 비표면적의 변화는 산 또는 염기의 반응으로 토양의 점토 입자 함량이 감소하였기 때문인 것으로 판단되며 (Panda et al. 2010), 또한 유기물의 용해도 비표면적 감소에 영향을 미친 것으로 판단된다.
3.2.2 유기물 함량
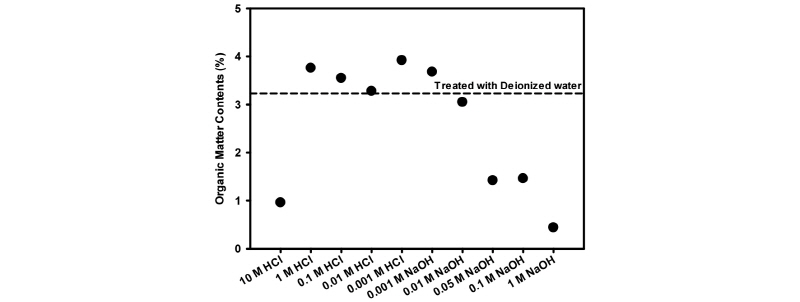
화학반응 이후 토양 유기물 함량은 Fig. 1과 같다. 1 M 농도 이하의 HCl 용액과 반응한 토양 유기물 함량은 기존의 함량인 3.23%와 차이가 0.6% 이내였으나, 1 M 이하의 NaOH 용액과 반응시킨 토양의 유기물 함량은 HCl 용액과 반응시켰을 때에 비해 상대적으로 차이가 크게 발생하였으며 NaOH 용액의 농도가 1 M일 때에는 유기물 함량이 0.44%까지 감소하는 경향을 보였다. 염기의 경우 fulvic acid와 humic acid를 모두 용해시킬 수 있으므로 상대적으로 낮은 농도의 염기와 반응하여도 토양 유기물 함량은 크게 감소하지만, 산의 경우 fulvic acid만을 용해시킬 수 있기 때문에 염기와 반응한 토양에 비해 유기물 함량 감소 정도가 낮은 것으로 판단된다 (Hillel and Hatfield 2005, Bohn et al. 2002).
한편, 산의 농도가 1 M 보다 큰 경우 염기와 반응한 경우와 마찬가지로 토양의 유기물 함량이 매우 크게 감소하였다. 10 M HCl 용액이나 1 M NaOH 용액과 반응한 토양 내 유기물 함량은 각각 0.96, 0.44%로 기존 토양 내 유기물함량인 3.23%에 비해 각각 약 30, 15% 정도로 크게 감소하였다. 10 M HCl 용액에서는 점토와 알루미늄 산화물의 용해로 인하여 Al3+의 농도가 크게 증가하였으며 (Table 3), Al3+는 humic acid 및 fulvic acid와 organometallic complex를 형성할 수 있다 (Hernández-Soriano 2012, Pandey at el. 2000). 10 M HCl 용액과 반응 시 organometallic complex 형성이 유기물 함량 감소에 영향을 미친 것으로 판단된다.
3.2.3 토양 pH
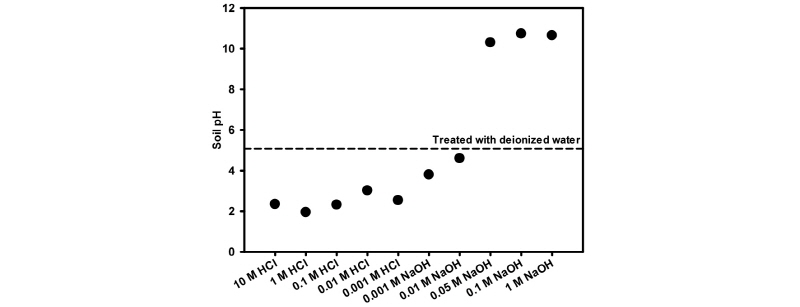
화학반응 이후의 토양 pH는 Fig. 2에 나타내었다. HCl과 반응한 토양의 경우, HCl 농도에 관계없이 pH 변화가 크게 나타나지 않았다. 특히 주입한 HCl 농도가 0.001 M에서 1 M 농도로 1000배 증가하였음에도 불구하고 토양 pH는 2.54에서 1.95로 적게 변화하였다. 반면에 NaOH 용액과 반응한 경우 0.05 M 농도 이상의 NaOH 용액에 대해서 완충능력이 급격히 감소되었으며, 특히 1 M NaOH 용액과 반응한 토양의 pH는 10.65로 화학반응 이전 토양 pH인 5.05에 비해 5 이상 증가하였다 (Fig. 2).
주목할 점은 NaOH 농도가 0.05 M 이상일 때 유기물의 용해 증가와 pH 완충효과 감소가 동시에 관찰되었다는 것이다. 이는 NaOH 농도가 0.05 M 이상인 경우 토양 유기물 (humic acid 및 fulvic acid)이 용해되어 완충효과가 현저히 감소하기 때문이라고 판단된다. 또한 10 M HCl 용액과 반응한 토양의 경우 유기물 함량은 크게 감소하였지만 pH는 변하지 않았는데, 이는 pH 2 부근의 토양에서 유기물뿐만 아니라 점토도 완충효과를 나타내기 때문이라고 판단된다 (Ulrich and Sumner 2012).
3.2.4 양이온교환능력 (CEC)
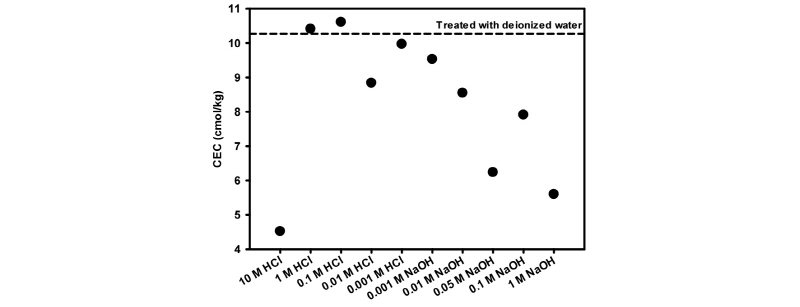
화학반응 이후의 토양 CEC 변화는 Fig. 3과 같다. 1 M 농도 이하의 HCl 용액과 반응한 토양의 CEC는 10.61 cmol/kg로 화학반응 이전의 CEC인 10.27 cmol/kg과 큰 차이를 보이지 않았으나, 10 M HCl 용액과 반응한 토양의 CEC는 4.52 cmol/kg로 화학반응 이전 토양의 CEC의 약 40% 수준으로 감소하였다. 한편 NaOH 용액과 반응시킨 토양의 CEC는 NaOH 용액의 농도가 1 M까지 높아짐에 따라 5.60 cmol/kg로 기존 값에 비해 50% 이하로 감소하였다.
상대적으로 NaOH에 의한 CEC 감소효과가 HCl에 의한 CEC 감소효과보다 더 높았으며, 이는 유기물 함량 변화와 일치했다. 즉 NaOH는 humic acid와 fulvic acid를 모두 용해시키는 반면 HCl은 fulvic acid만 용해시키므로 NaOH에 의한 유기물 함량 감소 정도가 HCl에 의한 유기물 함량 감소 정도보다 더 높았고, 이로 인해 NaOH에 의한 CEC 감소효과 역시 HCl에 의한 CEC 감소효과보다 더 높은 것으로 판단된다. 한편, 10 M HCl 용액과 반응한 토양의 유기물 함량은 0.96%로 1 M NaOH 용액과 반응한 토양 유기물 함량인 0.44% 정도만큼이나 크게 감소하였다. 10 M HCl 용액과 반응한 토양의 유기물 함량 감소가 CEC 감소에 큰 영향을 준 것으로 판단된다.
유기물의 표면전하는 pH에 따라 달라지며 pH가 증가할수록 표면 작용기의 수소 이온이 해리되어서 더욱 음전하를 띈다. 일반적으로 pH 5-8 범위에서 유기물의 CEC는 pH가 증가함에 따라 증가하는 경향을 보이지만 (Weil 2016), 본 연구에서 사용한 NaOH 용액은 0.001 M 농도를 제외하고는 모두 pH가 11이상이였으며, 해당 농도범위에서 유기물이 용해되어 CEC를 감소시키는 효과가 작용기에 존재하는 수소 이온의 해리로 CEC를 증가시키는 효과보다 더 큰 영향을 미친 것으로 보여진다.
3.2.5 치환성 양이온
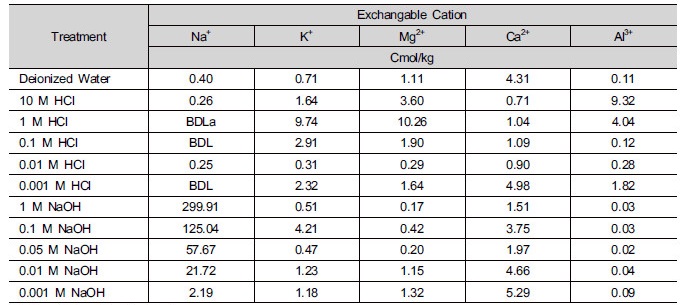
화학반응 이후의 토양 내 치환성 양이온 함량은 Table 3과 같다. 화학반응 이전에 치환성 양이온의 약 64.9%로 가장 많은 양을 차지했던 Ca2+는 HCl 및 NaOH 용액과 반응 시 쉽게 용탈되었으며 HCl 및 NaOH 주입농도가 각각 10, 1 M이었을 때 Ca2+의 농도는 4.31 cmol/kg에서 각각 0.71 및 1.51 cmol/kg으로 감소하였다. Mg2+는 1.11 cmol/kg에서 각각 3.60 cmol/kg 및 0.17 cmol/kg으로 변하였으며, K+는 0.71 cmol/kg에서 각각 1.64 및 0.51 cmol/kg으로 변했다. 또한 Na+는 0.40 cmol/kg에서 각각 0.26 및 299.91 cmol/kg으로, Al3+는 0.11 cmol/ kg에서 각각 9.32 및 0.03 cmol/kg으로 변했다.
토양 용액 내 H+의 농도가 높아질수록 토양에 정전기적으로 결합하고 있던 Ca2+가 H+로 치환되어 용탈되며 산과의 반응으로 점토 표면에 노출되어있는 Al3+가 용해된다 (Tyagi et al. 2006). Al3+은 강한 정전기적 인력을 통하여 토양에 결합하여 쉽게 용탈되지 않기 때문에 산성 용액과 반응하여서 토양의 산도가 높아질수록 치환성 양이온 중 Al3+의 함량이 늘어나게 된다. 이 경우 알칼리성 양이온 농도의 증감은 알칼리성 양이온이 용탈되어서 농도가 감소하는 효과와 점토 내부의 알칼
리성 양이온이 용해된 후 토양 표면과 결합하여 농도가 증가하는 효과의 경쟁으로 결정된다 (Tyagi et al. 2006). 반면, NaOH 용액과 반응한 경우에는 Na+의 치환으로 인해 다른 모든 치환성 양이온이 용탈된 것으로 보여진다. 또한 pH가 증가하기 때문에 용탈된 양이온이 수산화물을 형성하여 다른 치환성 양이온의 농도가 감소하는 효과도 있을 것이라 판단된다.
4. 고 찰
본 연구에서는 강산 (HCl)이나 강염기 (NaOH)와 반응한 토양 유기물 함량, pH, 치환성 양이온 함량 등의 변화를 살펴보았으며, 이러한 변화는 모두 육상생물의 생육에 악영향을 미치는 방향으로 진행되는 것으로 판단된다. 강산이나 강염기는 토양 유기물의 구성성분인 humic 및 fulvic acid를 용해시킬 수 있으며 (Bohn et al. 2002), 이로 인해 강산이나 강염기와 반응한 이후 토양 식물이나 지렁이의 영양분으로 사용되는 토양 유기물 함량이 감소하는 것으로 판단된다 (Fig. 1). 또한, 강산이나 강염기와 반응한 토양의 치환성 양이온 함량에도 큰 변화가 있었는데, 강산과 반응한 토양의 알칼리성 양이온 함량은 감소하고 알루미늄 이온의 함량이 증가하는 것으로 나타났다 (Table 3). 알칼리성 양이온은 토양생물의 필수 영양소로 사용되는 반면 (Bohn et al. 2002), 알루미늄 이온의 경우 토양생물에 독성을 발현하는 인자로 작용한다 (Bohn et al. 2002). 반면, 강염기와 반응한 토양에서는 나트륨 함량이 매우 높게 증가하였는데, 나트륨 농도가 매우 높아지면 토양생물에 독성이 발현될 수 있다 (Bohn et al. 2002).
본래 다양한 오염물질들을 흡착하여 저장고 역할을 하는 토양은 산・염기 물질과의 반응으로 표면 특성이 변화하게 되며 이로 인해 기존에 흡착되어 있는 물질이 용출될 수 있다. 뿐만 아니라, 산・염기 반응은 토양의 흡착 능력을 감소시켜서 후에 유입되는 오염물질이 쉽게 지하수로 유출될 수 있다. 산・염기 유출사고를 산・염기 물질의 고유한 유해성만으로 평가한다면 토양 특성 변화에 따른 생태학적 영향을 간과하게 되며 이를 고려한 위해성 평가를 실시하기 위하여 토양과 산・염기 물질의 반응 기작을 더욱 미시적인 관점에서 살펴보아야 할 것으로 판단된다.
5. 결 론
강산 혹은 강염기와 반응한 토양은 모래의 비율이 증가하며 실트와 점토의 비율이 감소하였고 이로 인하여 토성이 변하였다. 또한 동식물의 영양분인 유기물과 알칼리성 양이온이 감소하였으며 특히 강산과 반응한 토양은 식물독성에 관련된 알루미늄 이온의 함량이 크게 증가하였다. 환경부에 따르면 토양에 강산이나 강염기 물질이 유입된 경우 즉각적인 중화 조치를 취한다 (Ministry of Environment 2011). 그렇지만 이러한 중화 조치를 실시한다 하더라도 토양 내 유기물 함량 감소나 치환성 양이온 함량 변화 등 토양생태에 악영향을 유발할 수 있는 토양의 물리・화학적 특성 변화는 중화 후에도 지속적으로 잔류할 수 있다. 따라서 강산이나 강염기에 의한 화학사고가 발생하였을 때 즉각적인 중화 조치를 실시하였다 하더라도 토양생태에 영향을 미칠 수 있는 인자들에 대한 조사 및 조치 방안이 강구되어야 한다.