1. 서 론
2. 연구방법
2.1 수종 선발
2.2 토양 조성 및 중금속 처리
2.3 화분 조성 및 생육
2.4 생물량, 엽록소, 광합성, 항산화 및 납 함량 측정
2.5 통계처리
3. 결과 및 고찰
4. 결 론
1. 서 론
대한민국은 산업화와 도시화의 영향으로 여러 가지 환경오염 문제가 대두되고 있다. 특히 도시생태계의 경우 인구 증가, 차량의 증가와 다양한 경제활동에 따른 오염에 직면하고 있으며 자동차와 화석연료의 사용으로 중금속 농도가 증가하고 있다 (Ouellet and Jones 1983). 여러 중금속 중 납의 경우 채광, 금속가공, 살충제와 석유, 석탄의 연소는 물론이고 비료산업에서도 발생을 하여 대기 및 토양 오염을 일으키고 있다 (Verma and Dubey 2003). 특히 도심지에서 발생하는 가스형, 분진형 유해물질 중에 납의 함량이 높기 때문에 도심지나 도로변 토양에서는 납 농도가 증가하고 있다 (Yoo and Son 2003). 대한민국의 경우 과거에는 자동차 연료에 포함된 납이 대기와 토양에 심각한 오염을 일으켰고 (Park 1992), 이에 대처하기 위하여 무연휘발유 사용이 법제화 되었지만 이후 중국 등 주변 국가들의 오염된 가스 및 분진이 대기를 통해 확산 및 이동하면서 대기오염물질이 대한민국으로 유입이 되고 있는 실정이다 (Park et al. 2010). 황사를 포함하여 중국-몽고 지역에서 유입되는 먼지들이 대한민국 서울의 대기 중 납 농도에 큰 영향을 미치고, 납 입자의 토양으로의 건식 침식이 되는 주요 원인이며 (Han et al. 2004) 중국의 대기 오염문제는 차량의 증가, 도시화의 영향으로 갈수록 심각해지고 있어서 (Duan and Tan 2013) 대한민국도 영향을 받을 것으로 보인다. 따라서 대기 중 그리고 토양의 납 농도에 대한 지속적인 관심과 모니터링이 필요하며 이에 대응하기 위해 대한민국도 올해부터 미세먼지 중 납의 농도를 실시간 모니터링 및 정보공개를 하기 시작했다 (Choi 2015). 하지만 통계청 자료에 의하면 우리나라 국토 토양의 납 농도는 2011년 조사 기준으로 토양 1 kg 당 평균 35 mg이 들어 있어서 비록 각각 오염 기준농도는 다르지만 아연을 제외하고는 그 농도가 다른 중금속에 비해 높다 (카드뮴 0.68 mg/kg, 구리 32 mg/kg, 비소 7.36 mg/kg, 수은 0 mg/kg, 크롬 0.1 mg/kg, 아연 124 mg/kg) (KOSIS 2011). 또한 미국 환경보호청의 조류 대상의 토양 납 기준의 경우 11 mg/kg, 포유류의 경우 56 mg/kg 임을 (USEPA 2005) 감안하면 전국 평균이 35 mg/kg을 넘은 이 값은 우려되는 농도이다. 2014년도 연구에서도 경기도 지역에 납 오염이 심각한 지역이 다수 드러나는 등 대한민국 토양에서 납 오염은 지속적으로 문제가 되고 있다 (Lee 2014).
납은 경우 환경에 유입되면 분해되지 않고 오랫동안 여러 환경매체에 축적되어 장기간 잔류하게 되며 환경에 악영향을 끼치게 된다 (Park et al. 2010). 납의 경우 생태계에서 생물들의 생장 저해나 세포분열의 교란 등의 문제를 일으키고 (Ali et al. 2003) 식물에서 발아저해 생장 불량 및 생리적인 문제를 일으키는 중금속으로 (Verma and Dubey 2003) 알려져 있다. 그리고 납의 경우 식물농축도가 높아 세포질 단백질 형성에 큰 영향을 미치고 광합성까지 저해하여서 식물의 생장이 이루어지지 않는 문제점을 일으킨다 (Pourrut et al. 2011). 따라서 납 토양 오염이 크게 문제가 되는 도심지나 탄광, 공단 지역에 식재하는 식물의 경우 납에 대한 저항성이 높은 식물을 심는 것이 중요할 것이다. 그리고 납의 경우 식물의 활성산소에 영향을 미치기 때문에 (Pourrut et al. 2011) 식물을 저항성을 알아내기 위해 납에 대한 식물의 활성산소 반응을 고려한 식물의 반응 연구가 필요하다. 또한 토양에 축적되는 납의 농도를 줄이기 위해서는 잎에 축적되는 양도 높아서 토양의 납을 어느 정도 흡수-제거하는 것이 가능한지를 고려하는 것도 좋을 것이다. 따라서 본 연구에서는 가로수 수종으로 많이 쓰이고 있는 자생종 수목 4종을 대상으로 토양 내 납 농도에 대한 반응과 흡수능력을 연구하여 납 오염에 대응하는 가로수로 적합한 수종을 제시하고자 한다.
2. 연구방법
2.1 수종 선발
가로수 수종 중에서 외래종을 제외한 종들 중에서 대상종을 선발 하였다. 2009년 기준으로 서울시에 심어져 있는 가로수 중에서 1-4위를 차지한 은행나무 (Ginkgo biloba L.), 양버즘나무 (Platanus occidentalis L.), 벚나무 (Prunus serrulata var. spontanea (Maxim.) E.H. Wilson), 느티나무 (Zelkova serrata (Thunb.) Makino) 중에서 외래종인 양버즘나무를 제외하고 3종을 선발하였다 (Seoul City 2009). 다만 벚나무는 종묘회사에서 팔지 않는 관계로 왕벚나무 (Prunus yedoensis Matsum.)를 사용하였다. 그리고 같은 자료에서 2000년 이후로 식재 비중이 크게 늘고 있는 이팝나무 (Chionanthus retusus Lindl. & Paxton)를 추가적인 대상종으로 선발하였다. 연구에 사용된 식물은 과천묘목단지에서 구입하였으며, 크기가 비슷한 묘목을 골라 실험에 사용하였다. 나무의 평균 높이는 은행나무는 34.7 cm, 벚나무는 28.8 cm, 느티나무는 26.1 cm, 이팝나무는 29.7 cm 였고 구입시에는 잎이 나지 않은 상태여서 임시로 화분에 이식해서 1달 정도 온실에서 생육하여 어느 정도 잎이 자란 후에 사용하였다.
2.2 토양 조성 및 중금속 처리
실험에 사용한 토양은 서울 관악산에서 낙엽층을 걷어내고 채취하였으며 5 mm 체로 큰 나뭇가지나 잔돌을 걸러내었다. 사용한 토양의 유기물 함량은 8.8%였다 (n = 3). 토양의 납 함량은 12.4 mg/kg 이였고 시료 분석은 3반복을 실시하였다. 그리고 유기물 함량이 높은 토양임을 감안하여 생육 기간 동안 추가적인 시비는 하지 않았다.
각 처리구별 토양은 채집한 토양에 Pb(No3)2 용액을 첨가하여 (Deng et al. 2006) 납의 함량을 조절하였다. 대조구, 100 mg/kg, 200 mg/kg, 500 mg/kg, 1,000 mg/kg, 5,000 mg/kg의 6가지 처리구를 만들어 실험에 사용하였다. 100, 200 mg/kg 처리구의 경우 Pb(No3)2를 증류수에 녹여서 1,000 mg Pb / L의 용액을 만든 뒤 토양의 무게를 감안한 용액의 무게를 처리하여 사용하였다. 500, 1,000, 5,000 mg/kg 처리구의 경우 10,000 mg Pb / L 용액을 만들어서 사용하였으나 5,000 mg/kg 토양 처리구의 경우 이 농도를 맞추기 위한 용액을 다 투입하기 전에 토양이 물에 포화되어서 토양을 응달에서 건조 후 남은 용액을 한번 더 처리하였다.
토양환경보전법상 토양 내 납의 우려 기준은 1지역 (전, 갑, 과수, 목장용지, 주거용지, 학교용지 등등)의 경우 200 mg/kg, 3지역의 (공장, 주유소, 주차장 등) 경우 700 mg/kg 임을 감안하여 (KSEC 2009) 100, 200, 500 mg/kg 처리구를 이용하였고 이 농도는 실제 환경에서 출현 가능한 농도로 (environmental realistic level) 가정하였다. 고농도 처리구의 경우 미국환경보호청의 납에 대한 Eco-SSL (Ecological Soil Screening Level)의 납에 대한 screening level 중 가장 높은 값이 1,700임을 (USEPA 2005) 감안하여 1,000과 5,000 mg/kg 수준을 고농도 처리구로 설정하였다.
2.3 화분 조성 및 생육
5월 초에 상부 지름이 14 cm, 하부 지름이 10 cm, 높이가 15 cm 인 화분에 납을 처리한 직후 건조되지 않은 토양을 각각 2 kg 씩을 식물의 뿌리를 다치지 않게 조심스럽게 기존 토양과 바꾸어서 이식하였다. 이후 온실에서 10월까지 생육하였다. 화분에는 가상조건에 따라 일주일에 2-3회 포화수분함량 이하로 (토양 수분함량에 따라 100–200 ml 사이) 관수하였으며 간혹 용탈된 물의 경우 화분 받침에 모았다가 다시 화분에 주어서 납의 유실을 최소화하였다. 생육기간 동안 온실의 최대 온도는 38°C, 최저 온도는 19°C였으며 평균 기온은 26°C였다 (HOBO H9 tem-perature data logger; Onset, Bourne, MA, USA).
2.4 생물량, 엽록소, 광합성, 항산화 및 납 함량 측정
생물량은 10월에 각 개체의 잎을 전부 수거해 60°C 오븐에서 1주간 건조한 후 무게를 측정하였다. 엽록소는 SPAD-502 (Minolta Co., Japan)를 사용하여 측정하였다. 광합성의 경우 7월초에 맑은 날을 골라서 미국 LI-COR사에서 제작한 휴대용 광합성 측정기 LI-COR 6400 모델을 사용하여 측정하였다. 측정되는 잎에 일정한 광도를 제공하기 위하여 LED 광원 (LI-COR 6400-02)를 사용하였으며 (30°C, 400 ppm CO2) 측정 전날 물을 충분히 준 뒤 아침부터 오후 늦지 않은 시간까지 이틀에 걸쳐 측정을 하였다.
항산화 효소 측정은 식물의 잎을 흐르는 물에 씻은 후 실험용 종이타월을 이용해 물기를 제거한 후 잎을 따서 막자사발에 액체 질소를 이용하여 분말형태로 분쇄한 후 1:10 (w/v)의 비율로 50 mM potassium phosphate buffer (pH 7.5)에 넣고 원심분리하여 얻은 상등액을 항산화 효소의 활성을 측정하는 효소액으로 사용하였고, superoxide dismutase 활성은 SOD의 기질인 초산화물 음이온을(superoxide anion) 같이 분해시키는 WST-1(2-(4-Iodo-phenyl)-3-(4-nitrophenyl)- 5-(2,4-disulfophyenyl)-2H-tetrazolium, monosodium salt)을 사용하여 측정하였다 (Song and Lee 2010a).
토양, 뿌리 및 잎의 납 함량은 1 g의 건조된 토양과 식물을 60% HNO3 로 24시간동안 전처리 후 10 ml 70% 과염소산을 더하여 200°C 로 용액이 맑아질 때까지 가열하였다. 그 후 유도결합 플라즈마 방출분광기 (Model ICPS-1000Ⅳ )로 납 함량을 분석하였다.
2.5 통계처리
본 연구를 통해 얻어진 자료의 신뢰성 및 각 분석결과의 상관관계는 SAS 9.1 프로그램을 사용하여, 일원분산분석과 사후검정 (Tukey's HSD test)으로 분석하였다 (P < 0.05).
3. 결과 및 고찰
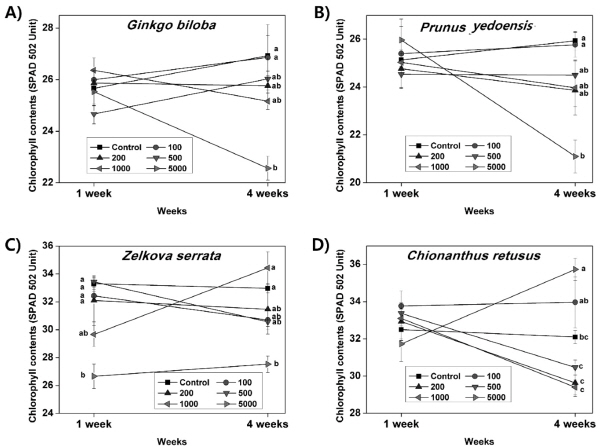
느티나무를 제외한 식물은 중금속 처리 후 1주후에 엽록소 함량의 변화가 없었지만 4주 후에는 모든 대상종에서 엽록소 변화가 나타났다 (Fig. 1). 느티나무의 경우 1주 후부터 고농도의 납 처리구 (1,000, 5,000 mg/kg)에서 엽록소 함량이 낮아졌지만 4주후에 1,000 mg/kg 처리구의 경우 회복이 된 반면에 5,000 mg/kg 처리구의 경우 엽록소 함량의 회복이 더딘 것을 알 수 있다. 은행나무와 왕벚나무의 경우 200 mg/kg 이상 농도의 처리구 모두 엽록소 함량이 유의하게 감소하였고 고농도로 갈수록 뚜렷한 경향을 보였다. 이는 납을 처리한 후 식물의 엽록소 반응을 관찰한 다른 연구와 비슷한 결과를 보이고 있으며 (Ewais 1997), 저농도 (50, 100 mg/kg)에서도 반응이 나타난 이 연구와 달리 100 mg/kg 의 농도에는 반응이 없는 것이 조금 다른 특징을 보이고 있다. 반면에 이팝나무의 경우 고농도로 갈수록 낮아지는 경향을 보이다가 5,000 mg/kg 처리구의 엽록소 함량이 유의하게 증가한 것을 볼 수 있다. 이는 실제로는 일부 잎이 건조해지는 과정에서 오히려 색이 짙어져게 나타났는데, 잎이 노란색으로 변하면서 천천히 시들지 않고 일부 잎들이 급격히 마르면서 엽록소는 파괴되지 않아서 높은 값을 보이게 된 것으로 사료된다 (Park et al. 2008). 실제로 이팝나무는 4주 동안 일부 잎이 말라서 떨어지는 현상을 보였다. 납의 경우 엽록소 합성과 관련된 식물의 단백질 대사에 영향을 주어 엽록소 함량을 낮추는 것으로 알려져 있는데 (Prasad and Prasad 1987) 본 실험에서 대상 종들의 경우도 이러한 스트레스를 받고 있는 것으로 나타났다. 그리고 이러한 스트레스는 생장량은 물론이고 식물의 항산화 작용에도 많은 영향을 미친다 (Pourrut et al. 2011). Table 1을 보면 은행나무를 제외한 모든 식물은 납 처리로 superoxide dismutase (SOD) 활성이 높아진 것을 확인할 수 있다. 이는 식물이 스트레스를 받고 있다는 것을 의미하며 다른 연구에서도 납을 처리한 식물의 SOD 값이 높아진 것과 (Sharma and Dubey 2005) 일치한다. 특히 엽록소 함량과 달리 항산화 효소의 경우 일부 식물 (이팝나무)에서 저농도인 100 mg/kg 처리구에서도 반응이 나타나서 식물 수종별 민감도를 확인 할 수 있었다. 그리고 고농도로 갈수록 값이 높아진 왕벚나무, 이팝나무와 달리 느티나무의 경우 200 mg/kg 부터 유의한 증가를 보이면서도 고농도에서 특별히 더 높아지지 않는 값을 보이고 있는데, 이는 이들 식물이 저농도에 대한 저항력은 높지 않지만 고농도에 대한 저항력은 상대적으로 다른 실험종에 비해서 높은 것을 의미한다 이는 Fig. 1에서 느티나무가 다른 나무들과 달리 고농도에서 엽록소 함량의 회복이 빠른 경향을 나타내는 것에 대한 원인일 가능성이 있다. 은행나무의 경우 항산화 효소의 반응에 유의한 차이를 보이지 않는데, 5,000 mg/kg 처리구의 경우 절대값의 차이는 있지만 오차가 커서 통계적으로는 유의한 차이를 보이지 않아서 이러한 결과를 보였을 가능성이 있다. 다른 가능성은 엽록소 함량의 경우에도 첫 주에는 통계적인 차이가 없다가 4주차에는 차이가 나는 점으로 미루어 납에 의한 영향 (스트레스)를 받지 않는 것은 아니지만 생리적인 반응이 느리게 나타나는 것일 가능성이 있는 것으로 판단된다.
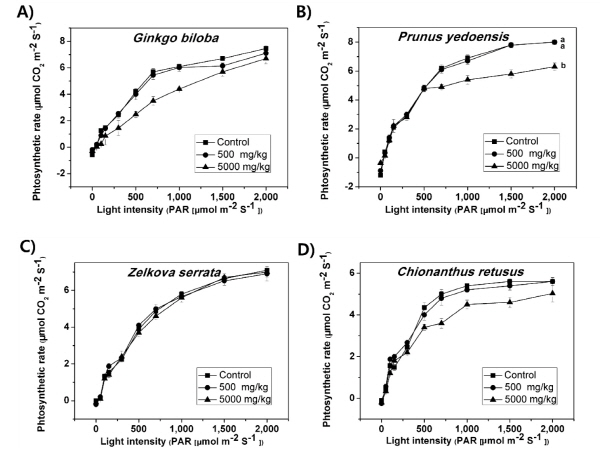
엽록소 함량을 보면 4주차에는 대부분의 식물이 납에 의한 영향을 받은 것으로 나타났지만 납 처리 후 2달후에 측정한 광합성량을 보면 벚나무를 제외한 대부분의 식물이 고농도에서도 영향을 받지 않는 것으로 나타났다 (Fig. 2). 벚나무의 경우 5,000 mg/kg 처리구에서 광합성량이 유의하게 감소한 것으로 나타났다. 광합성량 결과를 보면 식물들이 대부분 엽록소 함량이나 항산화효소 반응에서 보여진 납의 영향에서 많이 벗어난듯한 양상을 보여주고 있다. 이는 납이 점점 더 축적이 되면서 식물이 더 큰 영향을 받을 것으로 예측한 것과는 다른 양상을 보이고 있는데, 기존 중금속 함량이 높은 토양에서 수행한 연구에서도 3개월 정도 지난 후에는 식물의 항산화효소 반응이 정상으로 낮아진 것을 (Song and Lee 2010a) 관찰 할 수가 있었다. 중금속과 관련된 스트레스를 식물이 중금속을 액포 (vacuole) 등으로 이송하거나 스트레스성 손상 단백질의 복원, 외부 배출 등의 방법으로 독성을 완화하여 (Hall 2002) 납에 대한 스트레스를 줄여나갔을 가능성이 있다. 다만 본 연구와 같은 수종은 아니지만 비슷한 시기에 연구한 광합성량 연구에서는 대상 식물들이 1,000 PAR μmol m-2 s-1 의 광량을 전후하여 광포화가 뚜렷하게 나타난 반면에 (Song and Lee 2010a, Song and Lee 2010b), 이 연구에서는 음수인 이팝나무를 제외하고는 광포화가 일어나지 않는 차이점을 보이고 있다. 이는 식물이 스트레스를 받을 경우 광포화점이 높아진다는 (Ma et al. 1997) 다른 연구에 비교해 볼 때 처리구간 차이가 나타나지는 않았지만 식물들이 어느 정도 스트레스를 받고 있을 가능성이 있다.
최종적으로 잎의 생물량을 보면 은행나무를 제외하고는 5,000 mg/kg 처리구에서 식물이 납의 영향을 받았음을 알 수 있다 (Table 2). 이팝나무의 경우 큰 차이는 아니지만 500 mg/kg 처리구부터 납의 영향을 받는 것으로 보여 가장 납에 민감한 것으로 보이며 은행나무의 경우 고농도에서도 납의 영향이 나타나지 않았다. 하지만 대부분의 식물에서, 엽록소나 항산화 효소 반응에서는 납의 영향을 나타냈던 200-1,000 mg/kg 납 처리구에서 잎의 생물량이 대조구와 차이가 없는 경향을 보여줌으로써 식물들이 중기적으로 보았을 때 납 처리에 따른 독성을 극복했음을 알 수 있다. 연구 시작 전에는 키 생장량도 중요한 자료가 될 것으로 기대했지만 식물들이 키 성장은 거의 이루어지지 않았고, 특히 느티나무의 경우 목질화되지 않은 새로운 가지들이 많이 나면서 목질화된 부분의 생장은 거의 이루어지지 않았다. 이러한 점과, 앞에서 광포화가 나타나지 않은 점을 고려하면 중금속을 처리하지 않은 대조구 토양에서도 어느 정도 식물이 스트레스를, 특히 초기 스트레스를 받았을 가능성이 있는데 이는 이식과 관련된 스트레스 가능성이 있다. 이미 식물이 자라고 있는 토양에 중금속 처리를 하면 이러한 스트레스를 줄일 수 있지만 중금속을 용액 형태로 처리하면 식물의 뿌리 부분에 접촉하지 않고 토양 위 부분에 집중이 되는 (특히 저농도의 경우) 문제가 생길 수 있어 본 연구에서는 중금속 처리한 토양을 따로 만들어 이식을 했는데 이러한 점이 스트레스로 작용했을 가능성이 있다. 엽록소 함량이나 항산화효소 반응을 보면 중금속 처리구가 통계적으로 유의한 차이를 보이기 때문에 중금속의 영향은 증명이 되었지만 어느 정도는 이식에 대한 스트레스를 식물이 받았을 가능성을 배제할 수는 없다.
식물 뿌리의 중금속 함량은 중금속 흡수정도에 따른 식물 반응과 관련된 자료를 제공한다. Table 3을 보면 고농도로 갈수록 식물 뿌리의 납 함량이 높아져서 고농도의 토양에서 더 많은 납이 식물에 흡수되었음을 알 수 있다. 그리고 이 결과는 고농도로 갈수록 식물이 생리-생태적인 반응에서 유의한 차이를 보인 점을 설명해준다. 하지만 대조구의 토양이 12.4 mg/kg 이였음을 감안했을 때 각각 처리구별 식물 흡수량의 평균을 토양내 납 농도로 나눈 값을 비교해보면 대조구는 0.153, 100 mg/kg 처리구는 0.040, 500 mg/kg 처리구는 0.027, 5,000 mg/kg 처리구는 0.015로 고농도로 갈수록 흡수율은 떨어지는 것을 알 수 있다. 그리고 기존 연구를 보면 납의 경우 무거운 원소기 때문에 뿌리에 더 축적되거나 (KFS 2002) 뿌리 세포의 변형이 세포 내외로의 납 이동의 (apoplastic and symplastic Pb transport) 장벽으로 작용하여 뿌리에 더 높은 농도가 나온다고 보고되고 있으나 (Verma and Dubey 2003) 본 연구에서는 잎의 축적량과 (Table 4) 뿌리의 축적량이 (Table 3) 위 연구들에 비해서 큰 차이가 없었다. 잎의 흡수량을 뿌리의 흡수량으로 나누어보면 (translocation factor) 대부분 0.5-0.1 사이의 값을 보이고 있는데 (Table 5), 이는 주로 0.1-0.5 사이 값이 많이 나온 다른 연구들에 비하여 (Yoon et al. 2006; Verma and Dubey 2003) 높은 값을 보이고 있다. 뿌리의 흡수량에 비해 잎의 흡수량이 상대적으로 높다는 것은 그 식물들이 정화용 식물로서의 잠재력이 높다는 것을 의미하는데 (Yoon et al. 2006) 본 연구에서 은행나무의 경우 모든 처리구에서 0.7 이상의 값을 보이고 있다. 그리고 고농도 처리구인 5,000 mg/kg 처리구에서는 모든 식물이 0.9 이상의 값을 보이고 있는데, 이는 식물이 잎으로의 이동을 저지하도록 (Verma and Dubey 2003) 하기 보다는 잎의 액포로 이송하는 비율이 높아지는 것으로 추정된다 (Hall 2002). 이처럼 가로수로 활용하기 위해서는 납에 대한 저항성도 중요하지만 토양에서 납을 흡수하여 낙엽으로 배출해서 토양 정화를 시켜줄 수 있는 식물흡수 (phytoaccumulation) 능력도 중요할 것이다. 특히 이러한 식물흡수, 식물 정화는 저비용 고효율, 친환경적인 토양의 정화가 가능하고 (KFS 2002), 가을에 중금속을 함유한 낙엽을 수거함으로써 자연적으로 지속가능한 정화 시스템이 구축될 것이다. 따라서 잎의 납의 농도는 중요하고 특히 환경에서 출현 가능한 농도들에서 흡수량이 큰 의미를 지닐 것이다. 본 연구에서 제시하는 수종 별 납의 흡수량이 실제 환경에서 가로수로서의 토양 내 납의 식물추출 능력을 절대적으로 반영하는 것은 아니지만, 각 식물의 기본적인 능력을 반영하고 있을 것이다. Table 4를 보면 은행나무는 5,000 mg/kg 을 제외한 모든 처리구, 특히 실제 환경에서 나타날 수 있는 100, 200 mg/kg 처리구에서 가장 높은 납의 흡수-저장 능력을 보이고 있다. 따라서 실제 가로수가 심어져 있는 환경에서 좋은 흡수능력을 보일 것으로 기대된다. 벚나무의 경우도 낮은 농도에서 은행나무 다음으로 좋은 흡수능력을 보이고 있으며 이팝나무의 경우 저농도에서는 가장 낮은 흡수능력을 보이지만 5,000 mg/kg 처리구에서는 가장 높은 흡수능력을 보이고 있다. 본 연구는 2년 이하의 묘목이여서 실제 가로수로 식재되는 어느 정도 성장한 가로수 수종의 경우 흡수능력이 달라질 가능성이 있다. 하지만 목본 식물의 수종별 나이에 따른 흡수량을 비교한 참고 문헌은 찾을 수가 없어 예측이 힘들다. 그렇지만 본 연구에서 높은 묘목의 흡수량을 보여준 은행나무가 성체에서도 상대적으로 높은 가능성을 갖고 있을 것이다. 이러한 납 흡수 능력이 있는 가로수를 심고 잎을 수거하면 토양에 납이 축적되는 것을 어느 정도 예방할 수 있을 것으로 보인다.
4. 결 론
식물 엽록소의 경우 100 mg/kg 처리구에서는 대조구와 차이가 없고 항산화 효소의 경우에도 이팝나무를 제외하고는 차이가 없으며 광합성도 500 mg/kg 이하에서 차이가 나타나지 않는 것을 감안하면 실제로 대부분의 도심지에서는 토양내 납의 농도가 100 mg/kg을 넘지 않아서 대상종의 납 저항성은 큰 문제가 되지 않을 것으로 보인다. 미국 환경보호청의 토양 납 기준도 식물은 기준으로는 120 mg/kg 이기 때문에 (USEPA 2005) 전반적으로는 모든 수종에서 큰 문제가 없을 것으로 보인다. 하지만 대기 등을 통한 지속적인 중금속 축적이 일어난다던가, 오염 지역에서는 문제가 될 수 있을 가능성이 있기 때문에 이러한 점을 고려하면 은행나무가 연구 대상 종 중에서는 가장 납 오염에 대비하기 좋은 종이라고 할 수 있다. 또한 미국 환경보호청의 조류 대상의 토양 납 기준의 경우 11 mg/kg, 포유류의 경우 56 mg/kg 임을 감안하면 전국 평균이 35 mg/kg을 넘은 최근 국내의 값은 (KOSIS 2011) 이미 높은 수준이라 할 수 있다. 이러한 점을 고려하면 저항력뿐 아니라 저농도에서도 식물흡수 능력이 좋은 은행나무 같은 수종을 추후에 더 선발하여 가로수로 식재하는 것이 바람직할 것이다.