1. 서 론
광미는 선광 및 제련과 같은 광산활동을 통해 광체로부터 유용광물을 회수하는 과정에서 발생한다 (Jeong et al. 2015). 광미는 고농도의 중금속을 함유하고 있기 때문에 광산주변 수계 및 토양 오염의 주요 원인이 된다 (Park et al. 2006, Jeong et al. 2015). 경북 영덕군에 소재한 도곡광산 광미 내 중금속 함량은 Cd 133 mg kg-1, Cu 3,576 mg kg-1, Pb 8,807 mg kg-1, Zn 11,817 mg kg-1으로 보고된 바 있고 (Park et al. 2006), 경북 봉화군에 소재한 장군광산 광미 내 중금속 함량은 As 9,325 mg kg-1, Pb 946 mg kg-1, Zn 279 mg kg-1으로 보고된 바 있는데 (Jeong et al. 2015), 이는 대부분 토양오염대책기준을 초과하는 고농도이다. 일반적으로 광미는 광산 내 일정 지역에 적치되어 보관되는데, 광미 입자의 부유 또는 광미와 물/공기와의 접촉을 통해 생성된 산성광산배수 (acid mine drainage; AMD)를 통해 농경지 등의 주변 토양으로 확산되어 인체 및 생태계에 유해한 영향을 끼칠 개연성이 있다.
광미의 위해도를 저감시키기 위해 고형화/안정화 (Desogus et al. 2013)가 적용되고 있지만, 처리 후 광미에 대한 재이용 용도가 불분명하여 적치 또는 매립되고 있는 실정이다 (Bian et al. 2012). Acidithiobacillus ferrooxidans와 같은 철산화균을 이용하여 광미로부터 유용원소를 회수하기 위한 방안으로 활용되어온 생물학적 침출법 (bioleaching) 또한 광미의 위해도 저감기술의 하나로써 활용될 수 있다 (Bosecker 1997, Park et al. 2014, Nguyen et al. 2015). 생물학적 침출법은 약품 의존성이 적고 에너지원이 필요하지 않은 장점을 바탕으로 비교적 활발히 적용되고 있으나, A. ferrooxidans의 활성에만 의존해야 하기 때문에 온도와 같은 외부환경 변화에 매우 민감하다는 단점이 있다 (Ahonen and Tuovinen 1989, Bosecker 1997). 동전기 (electrokinetic) 공법 또한 광미의 위해도를 저감시키기 위한 방법으로 사용되고 있으나 (Baek et al. 2009, Kim and Kim 2001, Kim et al. 2001) 에너지원이 필요하여 경제적이지 못하다. 또한 안정화/고형화와 같은 기술은 광미 내 중금속의 농도가 유지되기 때문에 재용출에 의한 주변 환경오염의 개연성이 상존한다는 단점이 있다.
본 연구에서는 외부환경의 변화에 민감하지 않을 뿐만 아니라 광미 내 황철석 (FeS2)의 자발적인 산화반응을 촉진할 수 있는 화학전지 (연료전지)의 개념을 광미 무해화 공법의 일환으로 활용하고자 한다. 광미는 황철석을 비롯한 황화광물을 다량 함유하고 있는데, 황철석은 물 및 공기와의 접촉을 통해 자연적 (자발적)으로 산화되며 Fe3+과 황산이온을 생성하고 pH를 낮춘다. 황철석이 산화됨에 따라 낮아진 pH는 광미 내 중금속을 용출시킬 수 있다. 이러한 일련의 산화반응 속도는 화학전지의 개념을 도입함으로써 촉진될 수 있다. 전지의 음극부에서 황철석의 자발적인 산화반응 (즉, 갈바닉 산화)이 일어나며 이를 통해 생성된 전자가 전선을 통하여 양극부로 이동하여 환원반응을 일으키는데 (Logan 2008), 전선의 전기적 특성을 조절함으로써 산화반응의 속도를 제어할 수 있기 때문이다. 갈바닉 산화를 통한 광미 무해화 공법, 즉, 광미 내 중금속 용출량 제어공법은 화학약품의 투입이 없고, 에너지원이 필요하지 않을 뿐만 아니라, 외부환경의 변화에 민감하지 않은 공법이다.
따라서 본 연구에서는 갈바닉 산화를 통해 황철석의 용해 촉진 정도를 확인하고자 한다. 광산주변 수계 및 토양 오염을 유발하는 대부분의 광미에서 황철석의 존재가 확인되기 때문에, 황철석의 자발적 산화속도를 화학전지의 개념을 적용하여 촉진함으로써, 황철석 주위 pH를 효과적으로 변화시킬 수 있고, 그에 따라 광미 내 중금속의 용출량 또한 촉진할 수 있다. 본 연구에서 제안하는 황철석의 갈바닉 산화를 적용할 경우, 광미 내 중금속의 용출을 촉진시켜 제거할 수 있기 때문에, 처리 후 광미의 재이용 용도의 범위가 확장될 수 있다.
2. 재료 및 방법
2.1 황철석 준비
본 연구에서는 광산폐기물 내 황철석 성분을 모사하기 위해 페루산 자연 황철석을 사용하였다. XRD (X-ray diffraction, Bruker, Germany) 분석을 통해 불순물인 SiO2가 15% 함유된 황철석임을 확인했다. 막자사발을 이용하여 황철석을 분쇄한 후 0.5 N HNO3을 이용하여 분쇄된 황철석 표면의 철산화물을 세척하였다 (Bonnissel-Gissinger et al. 1998). 세척 후 체를 이용하여 입도 (d)가 250 μm ≤ d < 2,000 μm인 황철석을 분리하여 준비하였다.
2.2 갈바닉 반응기 제작
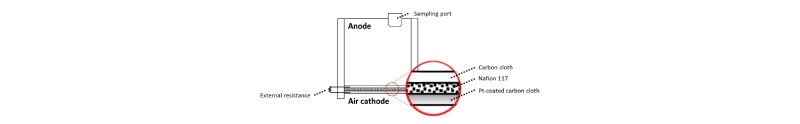
갈바닉 반응기는 음극부 반응기의 가로, 세로, 높이가 각각 5 cm이고, 공기와 닿아 있는 양극부의 형태 (air-cathode)를 가지도록 제작하였다 (Fig. 1) (Ju et al. 2015). 음극부와 양극부 사이에는 carbon cloth (0.35 mm, Ballard, USA), Nafion 117 (Dupont, USA), Pt-coated carbon cloth (0.5 mg-pt cm-2, 20 wt% wet proof, Ballard, USA)를 140°C에서 20 mPa로 3분 간 압착한 MEA (membrane electrode assembly)를 제작하여 사용하였다. 음극과 양극 사이에는 외부저항 (RExt = 1,000 Ω)을 연결하였다.
2.3 산성용액과 갈바닉 반응기 내 황철석 용해 반응
산성용액 내 황철석의 용해 반응을 위해 황산을 이용하여 pH 2로 조절한 산성용액 ((NH4)2SO4 3.0 g L-1, KCl 0.10 g L-1, K2HPO4 0.50 g L-1, MgSO4·7H2O 0.50 g L-1, Ca(NO3) 20.01 g L-1) 125 mL와 황철석 (20 g L-1)을 125 mL-Wheaton bottle에 넣고 23°C의 항온 조건에서 4주간 용해 반응이 일어나도록 하였다. 갈바닉 산화를 통한 황철석 용해반응을 위해, 갈바닉 반응기의 음극부에 동일한 산성용액 125 mL와 황철석 (20 g L-1)을 넣고, 23°C의 항온 조건에서 4주간 용해 반응이 일어나도록 하였다. 실험은 3반복으로 수행되었다.
2.4 측정 및 분석 방법
산성용액 및 갈바닉 반응기에서 황철석을 4주 간 반응시킨 후 산성용액과 반응기 내 액상시료를 채취하여 0.22 μm 필터로 여과한 후 ferrozine 방법을 이용하여 용존 이가 철 (Fe2+) 농도와 총 철 (total Fe)농도를 분석하였다 (Viollier et al. 2000). 용존 삼가 철 (Fe3+)의 농도는 ferrozine 방법을 이용하여 구한 총 Fe 농도에서 Fe2+농도를 빼서 산출하였다. 여과된 시료의 pH는 pH 전극 (8102BNUWP)이 장착된 pH 미터 (Thermo Fisher Scientific Orion 5-Star, USA)를 이용하여 측정하였다. 주사전자현미경 (SEM, Scanning Electron Microscope) (Hitachi S-4700, Japan)를 이용한 분석을 통해 황철석의 표면 모습을 관찰하였다.
3. 결과 및 고찰
3.1 갈바닉 산화를 통한 황철석 용해 후 황철석의 표면 변화
Fig. 2는 황철석의 산화 반응 4주 후의 표면 모습을 SEM을 이용하여 관찰한 결과를 보여준다. Fig. 2(a)는 실험에 사용한 황철석의 표면을 보여주고, Fig. 2(b)는 산성용액에서 반응한 황철석의 표면, Fig. 2(c)는 갈바닉 반응기 내에서 반응한 황철석의 표면을 보여준다. 산성용액 내에서 반응한 황철석의 표면 모습 (Fig. 2(b))과 달리 갈바닉 반응기 내에서 반응한 황철석 표면에서는 길쭉한 모양의 홈이 발견되었다 (Fig. 2(c)). 이는 Edwards et al. (2001)의 Fe3+에 의한 황철석 산화 실험 및 다른 연구자들이 bioleaching 후 황철석 표면을 SEM으로 관찰한 모양과 일치한다 (Mustin et al. 1992a, Mustin et al. 1992b). SEM을 이용한 황철석 표면관찰 중 산성용액 내에 있던 황철석의 표면 (Fig. 2(b))에서는 홈을 찾기 힘들었던 반면 갈바닉 반응기 내의 황철석 표면 (Fig. 2(c))에서는 다수의 홈이 발견된 것은 갈바닉 반응기 내에서 황철석의 용해가 산성용액 내 황철석의 용해보다 활발히 일어나고 있음을 보여 준다.
3.2 갈바닉 산화를 통한 황철석 용해
Fig. 3은 산성용액과 갈바닉 반응기 용액 내에서 4주 동안 황철석을 용해시킨 후 측정한 Fe 농도와 pH 결과를 보여준다. Total Fe의 농도를 비교한 결과 갈바닉 반응기 내 total Fe의 농도 (29.8 ± 7.4 mg L-1)가 산성용액 내 total Fe 농도 (10.3 ± 1.6 mg L-1)에 비해 평균 값 기준 약 2.9배 정도 높았다 (Fig. 3(a)). Fe3+의 농도를 비교한 결과, 갈바닉 반응기 내 농도 (27.6 ± 8.1 mg L-1)가 산성용액 내 농도 (6.0 ± 0.7 mg L-1)보다 평균 값 기준 약 4.6배 높았다 (Fig. 3(a)). 또한 갈바닉 반응기 용액 내 total Fe 중 92.7%가 Fe3+로 존재한 반면, 산성용액 내에서는 60.0%만 Fe3+로 존재하였다. 이를 통해 갈바닉 반응기 내에서 황철석의 용해뿐 아니라 용해된 Fe2+의 Fe3+로의 전환도 촉진됨을 알 수 있었다. 또한 산성용액 (pH 1.77 ± 0.01)보다 갈바닉 반응기 용액 (pH 1.54 ± 0.03)의 최종 pH가 더 낮았다 (Fig. 3(b)). 이는 갈바닉 반응기에서 황철석의 용해가 촉진되면서 생성된 수소 이온의 농도가 높아 pH가 더 감소했기 때문이라고 할 수 있다.
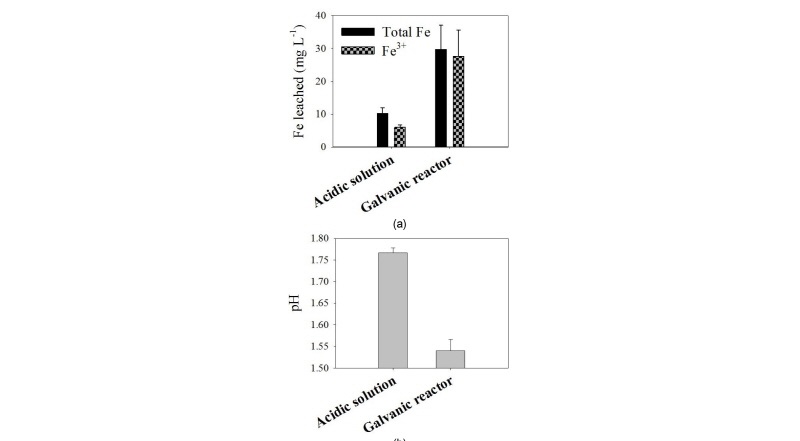
Fig. 3
Fe concentrations in the acidic solution (pH 2) and in the galvanic reactor (RExt = 1,000 W) (a) and final pH of the acidic solution and the galvanic reactor after pyrite dissolution for 4 weeks at 23°C (b). The data shows the average of triplicate samples, and error bars represent the standard deviation.
황철석 (FeS2)은 물에서 Fe2+와 S22-로 용해되고, 이 중 Fe2+ 는 Fe3+로 산화되면서 한 개의 e-를 생성하고, S22-는 SO42-로 산화되면서 14개의 e-를 생성하여 총 15개의 e-를 생성한다. 종합적으로 황철석은 물과 반응하여 산화하면서 Fe3+, 2SO42-, 16H+, 15e-를 생성한다 (Eq. 1) (Lowson 1982). 생성물 중 H+와 e-는 O2를 환원하면서 H2O를 생성한다 (Eq. 2).
FeS2 + 8H2O → Fe2+ + S22- + 8H2O → Fe3+ + 2SO42- + 16H++ 15e- (Eq. 1)
15/4O2 + 15H+ + 15e- → 15/2H2O (Eq. 2)
FeS2 + 1/2H2O + 15/4O2 → Fe3+ + 2SO42- + H+
(Eq. 3)
산성용액 내에서의 H+, e-의 이동과 갈바닉 반응기 내에서의 이동은 상이하다. 산성용액의 경우, 산성용액 내에서 황철석이 산화되면서 Fe3+, 2SO42-, 16H+, 15e-를 생성하고 (Eq. 1), 이 중 15H+-와 15e-가 산성용액 내 15/4O2를 환원한다 (Eq. 2). 결과적으로 산성용액 내에서는 황철석이 산화하면서 Fe3+, 2SO42-, H+가 생성된다 (Eq. 3). 갈바닉 반응기의 경우, 갈바닉 반응기의 음극에서 황철석이 산화되면서 Fe3+, 2SO42-, 16H+, 15e-가 생성된다 (Eq. 1). 이 중 15e-는 전선을 통해 음극에서 양극으로 이동하고, 15H+는 음극과 양극 사이에 위치한 수소이온교환막인 Nafion 117을 통해 이동한다 (Fig. 1). 이렇게 다른 경로를 통해 양극에 모인 15e와 15H+는 대기 중 15/4O2를 환원시킨다 (Eq. 2). 그리고 음극부 내에는 Fe3+, 2SO42-, H+가 잔류하게 된다 (Eq. 1 and Eq. 2).
산소에 의한 황철석의 산화에 관한 연구 (Williamson and Rimstidt 1994, Rimstidt and Vaughan 2003)에 따르면 황철석의 산화과정 중 생성된 전자가 전자수용체인 산소와 반응하는 과정이 황철석 용해에서의 율속과정 (rate-limiting step)이라고 한다. 갈바닉 산화를 통한 황철석의 용해 양이 산성용액 내 황철석의 용해양보다 많았던 것은, 갈바닉 반응기의 음극부에서 생성된 전자가 양극부의 O2와 반응한 것이, 산성용액 내에서 생성된 전자가 산성용액 내의 O2와 반응한 것보다 더 용이하게 일어났기 때문이라고 추정할 수 있다. Rimstidt et al. (1994)에 따르면 황철석 (FeS2)뿐만 아니라 황비철석 (FeAsS), 방연석 (PbS), 섬아연석 ((Zn, Fe)S), 황동석 (CuFeS2)과 같은 황화광물의 산화반응의 경우에도 전자수용체가 황화광물이 산화하면서 생성한 전자와 반응하는 것이 율속과정이라고 한다. 이는 황비철석, 방연석, 섬아연석, 황동석과 같은 황화광물을 함유한 광미에도 갈바닉 반응기의 적용을 통해 전자의 이동을 용이하게 하여 황화광물의 용해를 촉진시켜 황비철석으로부터 As, 방연석으로부터 Pb, 섬아연석으로부터 Zn, 황동석으로부터 Cu와 같은 중금속들을 용출시키고 동시에 pH도 저감시킬 수 있는 가능성을 보여준다.
4. 결 론
본 연구에서는 갈바닉 산화가 황철석의 용해를 촉진하고 이를 통한 pH 감소 효과를 가져오는지 비교 확인하기 위해, 갈바닉 반응기와 산성용액 내 황철석을 4주간 반응시킨 후 SEM을 이용한 황철석 표면을 분석하였고 용출된 total Fe와 pH를 비교하였다. SEM 분석을 통해 갈바닉 산화를 통한 황철석 용해시 길쭉한 모양의 홈이 생성되는 것을 확인하여 용해가 진행된 것을 확인하였다. 산성용액에 비해 갈바닉 반응기 내에서 2.9배 많은 total Fe가 검출되었고, pH가 더 낮은 것을 확인하였다. 본 연구를 통해 갈바닉 산화가 황철석의 용해를 촉진할 수 있음을 확인하였고, 이는 갈바닉 산화가 황화광물 함유 광미의 무해화 기술로 사용될 수 있는 가능성을 보여준다. 갈바닉 산화를 유도하기 위한 MEA (membrane electrode assembly)는 광미 적치 현장에 손쉽게 원위치 (in situ) 설치가 가능하다. 이와 같이, 갈바닉 산화의 적용은 약품 의존성이 적고, 에너지원이 필요하지 않기 때문에 친환경적 원위치 광미 무해화 기술의 하나로 활용될 수 있다.