1. 서 론
2. 연구 방법
2.1 비스페놀 A와 광촉매
2.2 광촉매 반응
2.3 화학 분석
2.4 물벼룩 급성독성 평가
3. 결과 및 고찰
3.1 광촉매 반응에 의한 BPA 분해제거
3.2 광촉매 반응에 의한 BPA 독성 변화
4. 결 론
1. 서 론
고급산화공정 (advanced oxidation process)은 수산화 라디칼 (hydroxyl radical)을 발생시켜 난분해성 및 미량 유해물질들을 처리하기 위한 공정으로 현재까지 활발히 연구되고 있다 (D'Oliveira et al. 1990, Cheng et al. 1995). 수산화 라디칼은 유기물과의 반응 속도가 매우 빠르기 때문에, 고급산화공정의 관건은 이러한 수산화 라디칼을 효율적으로 더 많이 생산하는데 있다 (Thomas 1965, Ishibashi et al. 2000, Chen et al. 2005). 고급산화공정은 자외선/과산화수소 공정, 오존 공정, 펜톤 산화 공정, 방사선 처리 공정, 자외선/광촉매 공정 등이 있는데, 이중에서 광촉매 반응은 친환경적인 방법으로 각광받고 있다.
광촉매 공정은 노닐페놀 (nonylphenol), 에스트라디올 (estradiol), 비스페놀 A (BPA, bisphenol A) 등의 내분비계 장애물질을 분해 제거할 수 있는 것으로 알려져 있다 (Chiang et al. 2004, Daskalaki et al. 2011, Jia et al. 2012). 특히, Jia et al. (2012)은 90분의 TiO2 (1.0 g L-1) 광촉매 반응 (자외선 파장 253.7 nm)으로 BPA (10 mg L-1)를 모두 분해 제거하였다고 보고하였다. 그러나 현재 광촉매 반응 연구는 오염물질의 분해 제거 효율에 집중되어 있으며, 광촉매 반응 전과 후 오염물질의 독성 변화에 대한 연구는 매우 제한적이다. Bistan et al. (2012)은 광촉매 반응에 의한 BPA의 제거율과 함께 에스트로겐 활성 및 독성 변화를 평가하였다. Degussa P25를 이용한 광촉매 반응 후 BPA가 대부분 제거되는 것을 확인하였지만, 처리 후 독성 결과는 시험종에 따라 차이가 있었다. 특히 물벼룩 유영저해율과 에스트로겐 활성은 처리 전 BPA 용액과 비슷한 수준으로 나타났지만, 발광박테리아의 발광저해율과 어류의 사멸율은 상대적으로 감소하였다.
본 연구에서는 광촉매 반응에 의한 BPA의 제거효율 평가하였으며, 이 반응에서 수산화 라디칼의 역할을 규명하였다. 특히 순수한 광촉매 반응에 의한 BPA의 분해제거를 평가하기 위하여 광분해 반응, 가수분해 반응, 흡착 반응에 의한 영향도 함께 고려하였다. 그리고 수계에서 먹이사슬의 중간단계를 대표하는 수서무척추동물의 일종인 Daphnia magna를 이용한 급성독성평가를 수행하여 광촉매 반응 처리 전과 후 BPA의 독성 변화를 확인하였다.
2. 연구 방법
2.1 비스페놀 A와 광촉매
본 연구에 사용된 비스페놀 A (BPA, ≥99%)는 Sigma-Aldrich 사 (USA)의 제품을 구입하여 정제과정 없이 사용하였다. 시험 용액은 탈이온수 (Puris Esse- UP ultrapure water System, Mirae St Corp., Korea)를 이용하여 고농도의 표준용액을 제조한 후 실험 전 초기농도를 1.0×10-5 M로 희석하여 실험에 사용하였다. 해당 농도는 기존의 연구결과와 수환경 중에 존재하는 일반적인 농도를 바탕으로 선정하였다. 제조한 용액의 농도를 확인하기 위하여 고성능 액체크로마토그래프 (HPLC-PDA, Waters 515, USA)로 분석하였으며, 초기 농도 확인 후 실험을 수행하였다.
광촉매 반응 실험에서 사용한 촉매는 TiO2로, 상용화 되어 있는 Degussa P25 (Germany)를 구매하여 사용하였다. Degussa P25는 anatase 80%, rutile 20%로 구성되어 있으며 크기는 21 nm, 비표면적은 51 m2 g-1이다.
2.2 광촉매 반응
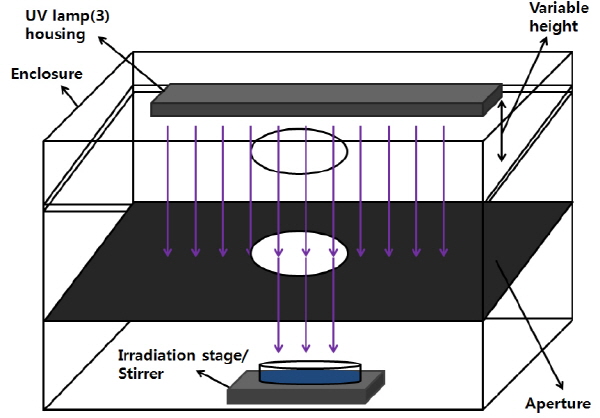
본 연구에서는 평형 조사 장치 (collimated beam device)를 광촉매 반응기로 사용하였다. 반응기는 비순환 형태의 회분식 반응 시스템으로, 광촉매 반응 실험 시 동일한 실험 조건을 충족시키기 위하여 광량 조절과 외부 빛 차단 등을 고려하여 개조하였다 (Fig. 1). 반응기 내부는 자외선 조사부, 자외선을 집중시키는 조리개 역할을 하는 칸막이, 광량을 조절할 수 있으며 샘플이 조사될 수 있는 시료부로 구성하였다. 또한 반응물질의 흡착과 자외선 방출을 막기 위하여 반응기를 스테인레스 스틸로 제작하였으며, 외부 빛이 차단될 수 있도록 암막을 이용하여 빛의 투입을 최소화하였다. 자외선 조사는 365 nm의 파장을 가지는 black light UV lamp (TL-D 15W/08, 45 cm, Philips, Netherlands) 3개를 사용하였으며, 조사 강도는 자외선 광량 측정기 (UVX-365 radiometer, UVP Inc, CA, USA)를 이용하여 3,000 μW cm-2가 되도록 실험 시작 전 조절하였다.
광촉매 반응 실험은 BPA 시험 용액 50 mL와 광촉매인 TiO2 (2.0 g L-1)를 유리 비커 (Pyrex® glass petridish)에 넣고 실시하였다. 광촉매 반응이 진행되는 동안 반응물질들을 완전히 혼합시키기 위하여 반응기 하부에 교반자를 넣고 충분히 교반하였다. 자외선 조사 전에는 15분 동안 암 조건에서 시료를 교반하여 광촉매에 대한 BPA의 흡착을 평가하였다. 총 자외선 조사 시간은 3시간으로 하였으며, 시료 채취는 자외선 조사 0, 15, 30, 60, 120, 180분에 각각 실시하였다. 채취한 시료의 총 용량은 초기 시료양의 5 v/v%를 넘지 않도록 하였다. 시료 채취 후 BPA 화학분석과 독성평가를 수행하기 위하여 0.45 μm 실린지 필터 (Millex-HV syringe filters, PVDF, Bedford, USA)을 사용하여 광촉매를 여과하였다. 그리고 독성평가 시료는 1 M HCl과 1 M NaOH 를 이용하여 pH를 적절한 수준으로 조절하였다.
광촉매에 의한 BPA의 흡착을 평가하기 위하여 회분식 흡착 실험을 실시하였다. 흡착 반응은 광촉매 반응과 동일하지만 자외선을 조사하지 않은 암 조건에서 평가하였다. 그리고 자외선 조사와 광촉매가 없는 암 조건에서 가수분해 반응을, 광촉매를 넣지 않고 자외선만 조사한 조건에서 광분해 반응을 각각 평가하였다. 한편, 광촉매 반응에서 수산화 라디칼의 역할을 규명하기 위하여 소광제인 메탄올을 첨가하여 BPA의 광촉매 반응을 실시하였다. 그리고 광촉매 반응의 동력학을 유사 1차 반응으로 해석하고 초기 반응 속도 상수를 산출하였다.
2.3 화학 분석
BPA 농도는 HPLC (High Performance Liquid Chromatography, Waters 515, USA) 시스템을 이용하여 분석하였다. 분석용 컬럼은 Nova Pack C18 reverse phase column (150 mm × 9.9 mm × 4 μm, Waters)을 사용하였으며, PDA (Photodiode Array, Waters 2996, USA) 검출기를 이용하여 측정하였다. 시료는 20 μL를 유속 1 min L-1로 고정하여 주입하였으며, 이동상은 water:acetonitrile = 55:45을 사용하여 226 nm에서 검출하였다.
독성평가 시험 용액의 수소이온 (pH)과 용존산소 (DO) 농도는 각각 pH meter (Orion 3 star portable- 8103BN, Thermo scientific, USA)와 DO meter (Orion DO/BOD meter 862A, Thermo scientific, USA)를 이용하여 측정하였다. 그리고 광촉매 반응에 의한 BPA의 무기화 (mineralizaion)을 확인하기 위하여 총유기탄소 (TOC) 농도를 TOC Analyzer (TOC-V CPH, SHIMADZU, Japan)로 측정하였다. 모든 분석은 3회 반복하였으며, 결과는 평균값과 95% 신뢰수준으로 표기하였다.
2.4 물벼룩 급성독성 평가
광촉매 처리 전과 후의 독성변화를 평가하기 위하여 물벼룩 (Daphnia magna)을 이용한 급성독성시험을 OECD guideline 202에 준하여 수행하였다 (OECD 2004). 산란용 어미의 사육을 위하여 OECD 시험기준에 따라 제조된 배양액을 사용하였고, 먹이는 담수녹조류인 Chlorella vulgaris를 희석하여 공급하였다. 물벼룩 급성독성 평가에는 최소 3회 이상 어린 개체를 생산한 성체에서 생산된 생후 24시간 미만인 어린 개체를 사용하였다. 시험기간 동안 먹이는 주지 않았으며, 온도 20±2°C, 광주기는 16시간의 광조건과 8시간의 암조건을 유지하였다.
독성평가는 50 mL 유리비커에 시료 10 mL와 물벼룩 5마리를 넣고 4회 반복 실험하였다. 시료는 희석수를 사용한 대조구와 함께 처리수 100%를 기준으로, 50%, 25%, 12.5%, 6.25%를 사용하였다. 희석수는 (pH=7.8±0.1, 경도=250±25 mg L-1 as CaCO3) ISO에서 제시한 용액을 사용하였다 (ISO 2012). 급성 독성은 24시간과 48시간 후의 물벼룩 유영저해율 (immobilization, %)을 확인하여 평가하였다. 유영저해는 시험 용기를 살며시 움직여주고 15초 후 관찰했을 때 일부 기관(촉각, 후복부 등)이 움직임이 없거나 유영하지 않을 때, 그리고 촉수를 움직인다 하더라도 유영을 하지 못하는 경우로 판단하였다.
물벼룩의 50%가 유영저해를 일으키는 농도 (EC50)는 독성시험 결과 유형에 따라 Graphical, Probit method와 Trimmed Spearma-Kaber method를 사용하여 산출하였으며 (Weber 1991), 이를 다시 독성단위 (TU=100/EC50)로 환산하였다. 광촉매 반응 처리 전과 후의 독성 비교는 paired t-test을 사용하였고, p 값이 0.05 이하일 경우 유의한 것으로 판정하였다 (SAS System, Version 9.4, SAS, USA).
3. 결과 및 고찰
3.1 광촉매 반응에 의한 BPA 분해제거
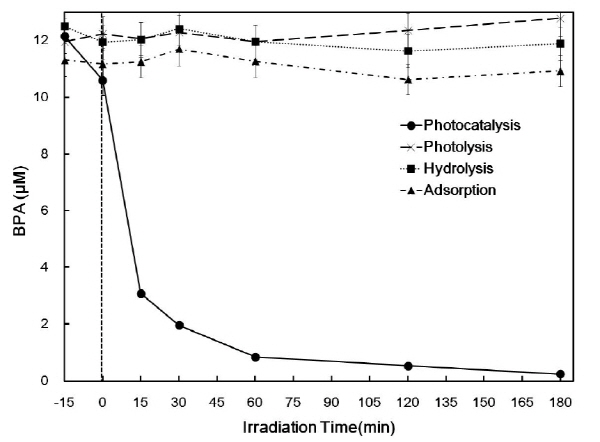
180분간의 광촉매 반응에 의한 BPA (1.0×10-5 M)의 분해제거 결과는 Fig. 2에 나타나 있다. 대조군으로 광촉매를 첨가하지 않고 자외선만을 조사한 광분해 반응, 암조건의 가수분해 반응, 자외선 조사 없이 광촉매만 첨가한 흡착 반응의 BPA 제거율은 각각 2%, 5%, 13%로 나타났다. 이에 반해 광촉매 반응에 의한 BPA의 제거율은 98%로 나타났으며, 60 분 이내에 빠르게 진행되었다. 이러한 결과는 광촉매 반응을 제외한 다른 반응들이 BPA의 분해제거에 큰 영향을 주지 않았다는 것을 보여준다. Tao et al. (2011)은 TiO2 나노입자 광촉매 반응에 의한 BPA의 저감을 연구하였는데, 자외선 60분 조사 후 BPA의 농도가 60% 정도 감소하였다고 보고하였다. 그리고 Wang et al. (2009)은 Daegusa P25를 이용하여 광촉매 반응에 의한 BPA의 제거율을 평가한 결과, 자외선 조사 60분 이내에 BPA가 대부분 분해되는 것을 밝혀내었다. 상기의 연구들은 광촉매에 의한 BPA의 흡착 제거를 확인하지 않았는데, 본 연구 결과 BPA의 광촉매 흡착은 13% 정도로 광촉매 반응에 의한 제거율 보다 매우 낮은 것으로 나타났다. 한편, 광촉매 없이 자외선 조사만으로도 BPA의 분해가 일어나지만 광촉매와 함께 자외선을 조사 하였을 때 99%에 가까운 제거효율을 보였다고 보고되고 있다 (Jo 2004).
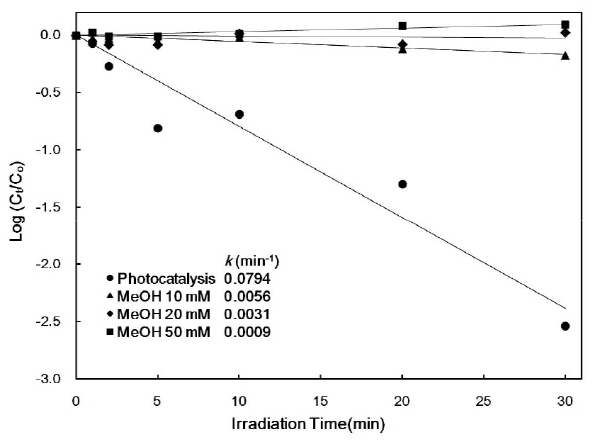
일반적인 산화 조건의 광촉매 반응에서 유기오염물질은 가전자대에 발생된 양공 (h+)과 수용액 속의 물분자나 수산화 이온이 반응하여 생성된 수산화 라디칼 (‧OH)과 반응하여 제거된다고 알려져 있다 (Linsebigler et al. 1995, Fujishima et al. 2000). 그러나 일부 연구에서는 양공이 광촉매 표면에 흡착된 유기오염물질과 직접 반응하여 산화시킨다고 보고하고 있다 (Matthews 1986). 그러나 본 연구에서는 BPA의 광촉매 흡착이 크지 않다는 것을 고려하면, BPA는 대부분 수산화 라디칼과 반응하여 산화 분해되었음을 추측할 수 있다. Fig. 3은 BPA의 광촉매 반응에 미치는 메탄올의 영향을 나타낸 결과이다. 메탄올은 수산화 라디칼 소광제로 활용되는 물질로서 본 연구에서 사용한 광촉매인 TiO2에 대한 흡착이 매우 낮은 것으로 알려져 있다 (Chen et al. 2005). BPA의 제거 속도는 메탄올 농도가 증가할수록 감소되는 것으로 나타났으며, 특히 BPA 농도보다 5000배 이상의 메탄올을 첨가하면 BPA가 거의 제거되지 않았다. 이것은 수산화 라디칼과의 반응이 BPA 분해제거의 주요 기전임을 의미한다. Ji et al. (2013)은 메탄올 소광 실험을 통하여 TiO2 광촉매 반응에 의한 아테놀올 (atenolol)의 분해에서 수산화 라디칼이 중요한 역할을 한다고 보고하였다. 한편, BPA 제거율 (Ct/Co)의 log 값과 반응 시간은 선형 관계를 보여 주었으며 (Fig. 3), 이를 통하여 BPA가 유사 1차 (pseudo- first order) 반응으로 제거됨을 알 수 있다. BPA의 농도가 90% 제거되는 시간 (25분)을 기준으로 산출한 초기 반응 속도 상수 (k)는 7.94×10-2 min-1으로 나타났다.
3.2 광촉매 반응에 의한 BPA 독성 변화
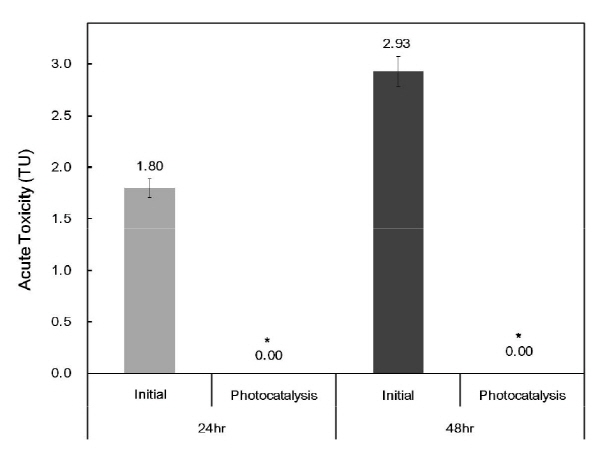
광촉매 반응에 의한 BPA의 독성 변화를 관찰하기 위하여 물벼룩인 D. magna을 이용하여 급성독성 평가를 실시하였다 (Fig. 4). 물벼룩에 대한 BPA (1.0× 10-5 M)의 24시간과 48시간 급성독성은 초기 각각 1.80과 2.93 TU이었으며, 180분간의 광촉매 반응에 의하여 BPA 독성이 모두 제거된 것으로 나타났다. Brennan et al. (2006)은 D. magna에 BPA의 48시간 반수영향농도 (EC50)가 7.75×10-3 g L-1라고 보고하였으며,Caspers (1998)는 D. magna에 대한 BPA의 무영향농도 (NOEC)를 3.16×10-3 g L-1로 보고하였다. 180 분간의 광촉매 반응 후 잔존하는 BPA의 농도가 5.47×10-4 g L-1임을 고려할 때, BPA에 의한 D. magna의 독성 영향은 무시할 수 있을 것으로 판단된다.
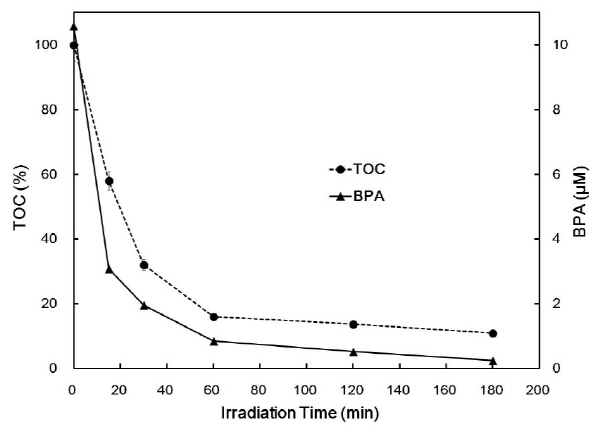
광촉매 반응에 의한 총유기탄소 (TOC) 제거율 측정을 통하여 BPA의 무기화를 조사한 결과는 Fig. 5에 나타나 있다. BPA의 무기화는 60분 이내에 대부분이 진행되었으며, 180분간의 광촉매 반응에 의하여 89%의 TOC가 제거되었다. 이것은 BPA가 제거되는 경향과 유사하였으며, 대부분의 BPA가 무기화되어 중간산물의 생성이 많지 않다는 것을 나타낸다. 따라서 광촉매 반응에 의하여 독성물질인 BPA가 무영향농도에 가깝게 분해 제거되었으며, 독성을 가진 분해산물이 생성되지 않아 물벼룩에 대한 독성이 발현되지 않은 것으로 판단된다. 한편, Yeo and Kang (2006)은 TiO2를 이용한 BPA의 광촉매 반응 후 지브라피쉬 (Danio rerio)의 수정란 부화율이 대조군과 유사해지는 것을 확인하였다.
4. 결 론
BPA는 TiO2 나노입자를 이용한 광촉매 반응에 의하여 효과적으로 분해 제거되었으며, 이 반응에서 가수분해, 광분해 및 흡착 반응은 무시할 정도였다. 그리고 BPA의 주요 제거 기작은 수산화 라디칼과의 반응이며, 유사 1차 반응으로 설명되었다. 한편, 광촉매 반응에 의한 BPA의 분해 제거 후 물벼룩에 대한 급성독성은 완전히 제거되었다. 이를 통하여 TiO2 나노입자를 이용한 광촉매 반응이 유해물질 분해 제거를 위한 고도처리 공정으로 안전하다는 것을 확인할 수 있었다. 그러나 처리수의 생물독성은 민감성이 다른 시험종에 따라 차이가 있으므로, 다양한 시험종을 이용한 처리수의 독성평가가 추가적으로 필요하다고 생각한다.