1. 서 론
2. 재료 및 방법
2.1 Naphthoquinone 계열의 살조물질
2.2 조류 배양
2.3 최우수 살조물질 선정을 위한 살조효과 평가
2.4 최우수 살조물질의 살조 범위 및 최적 농도 선정
2.5 생태독성 평가
2.5.1 급성 독성평가
2.5.2 D. magna를 이용한 만성 독성평가
3. 결 과
3.1 남조류 제어 가능한 화합물 선정을 위한 살조효과 평가
3.2 살조물질의 살조 범위 및 최적 적용 농도 평가
3.3 생태독성 실험
3.3.1 급성 생태독성 평가
3.3.2 만성 생태독성 평가
4. 고 찰
5. 결 론
1. 서 론
유해 남조류 대발생 (CyanoHABs, cyanobacterial harmful algal blooms)은 이들의 생육 서식지에 따라 환경적, 보건학적, 산업적으로 다양한 문제를 일으키고 있다. 호수, 하천, 저수지, 양어장 등에서의 유해 남조류 대발생은 수계 내 수생생물의 폐사를 일으키며 (Duke et al. 2002), Dolichospermum 종을 포함한 유해 남조류의 대발생 시 상수원에 흙 냄새 (off- flavor)를 발생하여 수자원 확보의 문제를 일으키고 있다 (Hobson et al. 2010, Zamyadi et al. 2015). 그리고, 물의 착색 및 스컴 (scum) 형성 등으로 불쾌감을 유발하고 여가 및 산업 활동을 저해하며, 상수 처리과정 중 여과지 폐쇄 및 응집 침전 저해 등으로 인한 경제적 손실을 야기한다. 더불어, 유해 남조류 Microcystis, Dolichospermum, Aphnizomenon 속의 대부분은 유해 독소인 Microcystin, Anatoxin 및 Saxitoxin을 생성하여 사람 및 동물에 유해한 영향을 미친다고 보고되어 있다 (Codd et al. 2005).
이러한 유해 남조류 대발생에 의한 피해를 막기 위해 생물학적, 물리학적, 화학적 방법 등의 다양한 제어 기술들이 개발되어 사용되었으나, 현재까지 현실적으로 현장에서 적용 가능한 기술은 화학물질을 살포하는 방법뿐이다. 하지만, 이런 화학물질을 이용한 제어 기술 역시 수 생태계 및 저질층에 축적되어 생태독성의 잠재적인 문제점을 갖고 있어 현장적용의 어려움이 지속적으로 발생하였다 (Park et al. 2001). 또한, 현재 국내・외에서 주로 사용되는 응집제 및 탈인제를 이용한 유해 남조류 제어 기술 역시 대상조류 이외의 다른 수생 생물에 영향을 미쳐 수생태계가 파괴되었다 (Lim et al. 2002, Yamamoto et al. 2005, Lürling and Oosterhout 2013). 따라서, 본 연구진은 앞선 문제점이 보완된 보다 친환경적인 유해 남조류 제어 기술을 개발하고자 자연계에 존재 혹은 생물로부터 유래된 물질을 대상으로 새로운 살조물질을 개발하고자 하였다. 자연계 혹은 생물 유래 물질의 경우, 상대적으로 생태계에서 자연분해가 되기 쉽고, 인간 및 동물에게 독성이 나타날 가능성이 적다. 본 연구에서 사용한 Naphthoquinone (NQ) 물질 역시 다양한 식물 (cf. Droseraceae, Juglandaceae, Nepenthaceae, Plumbaginaceae)과 미생물 (Streptococcus faecalis)에서 생성 혹은 자연계 존재하는 물질이며, 항암제 (antitumor), 항염증제 (anti-inflammatory), 항알레르기제 (antiallergic), 말라리아 치료제 (antimalarial) 등의 기능으로, 의약품의 원료로 사용되며, 다양한 세균, 곰팡이 등에도 효과적인 제어 효과를 나타내어 다방면에서 사용이 되고 있는 물질이다 (O’Brien 1991, Monks et al. 1992, Dong et al. 2009, Menna-Baretto et al. 2009). 따라서, 본 연구진은 NQ를 기반으로 하여 다양한 치환기 (Rn)를 변화시켜 합성한 살조물질의 효과 및 생태계 미치는 영향에 대하여 평가하였다. 하지만, 기존 연구는 겨울철 녹조 현상의 원인 종인 Stephanodiscus hantzschii을 대상으로 한 연구로써 (Byun et al. 2015, Joo et al. 2015), 여름철 국내에서 발생하여 가장 큰 문제점을 일으키는 유해 남조류 Microcystis, Dolichospermum에 대한 NQ 물질의 살조효과 평가는 이루어 지지 않았다.
따라서, 본 연구에서는 유해 남조류 Microcystis, Dolichospermum 속을 제어하기 위해 NQ 기반 물질의 살조효과를 평가하였고, 최종 선정된 살조물질의 현장 가능성을 평가하기 위해 살조범위와 생태독성 연구를 수행하여 실제 현장 적용이 가능한 친환경적인 살조물질을 개발하고자 하였다.
2. 재료 및 방법
2.1 Naphthoquinone 계열의 살조물질
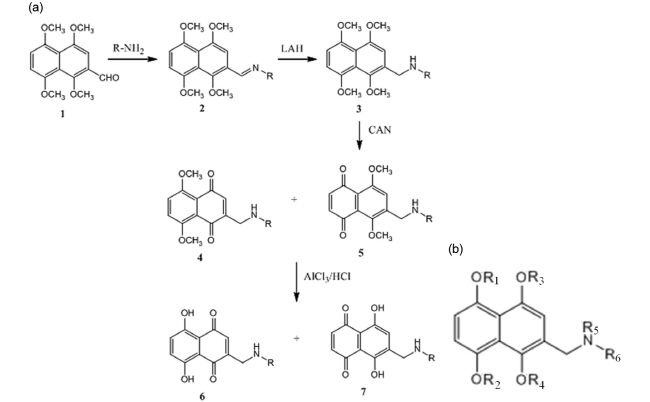
Naphthoquinone (NQ) 유도체의 기본적인 화학적 구조와 합성 과정은 Fig. 1에 표시하였다. Toluene을 용매로 하여 triethylamine 존재 하에서 2-formyl-1,4,5,8- tetramethoxynaphthalene과 amine을 반응시켜 N-(R)- N-[(1,4,5,8-tetramethoxy-2-naphthyl) methylidiene] amine (2)를 합성한다. 화합물 N-(R)-N-[(1,4,5,8- tetramethoxy-2-naphthyl) methyl] amine (3)의 합성은 lithium aluminum hydride (LAH) 또는 NaBH4로 처리함으로써 얻을 수 있다. 화합물 3을 산화제인 CrO3 또는 CAN으로 처리하여 화합물 2-{[(R) amino] methyl}-5,8-dimethoxynaphthalene-1,4-dione (4), 6- {[(R) amino] methyl}-5,8-dimethoxynaphthalene-1,4- dione (5)를 합성한다. 계속해서 화합물 4와 5를 AlCl3 및 HCl로 처리하여 최종물질인 화합물 2-{[(R) amino] methyl}-5,8-dimethoxynaphthalene-1,4-dione (6), 6-{[(R) amino] methyl}-5,8-dimethoxy-naphthalene-1,4-dione (7)을 합성한다. Naphthoquinone 기본골격을 기반한 살조물질은 기본 구조에 치환기 (Rn)를 다양하게 변화시켜 총 92종의 화합물을 합성하였다. 모든 화합물은 조선대학교 응용화학소재공학과 조 훈 교수팀 연구실에서 합성하여 제공받았다.
2.2 조류 배양
본 연구에 사용된 식물플랑크톤은 총 5종으로 남조류 Dolichospermum flos-aquae, Microcystis aeruginosa 2종, 규조류 Stephanodiscus hantzschii, Cyclotella meneghiniana, 2종, 와편모조류 Peridinium bipes 1종으로, Microcystis aeruginosa NIES 298는 일본 NIES (The National Institute for Environmental Studies, Japan), Dolichospermum flos-aquae CCAP 1403/13B은 영국의 CCAP (Culture collection of Algae and Protozoa)로 부터 분양 받았다. Stephanodiscus hantzchii UTCC 267은 캐나다 UTCC (The University of Toronto Culture Collection of Algae and Cyanobacteria, Canada), Cyclotella meneghiniana HYK0210-A1의 경우는 경안천 (Kyeongan Stream)에서 직접 분리한 조류를 사용하였다. Peridinium bipes HYJ0511-03의 경우 전라남도 주암천 (Juam Stream)으로부터 분리되었다. 남조류의 경우 CB (NIES 2004) 배지, 20˚C, 30-40 μmol m-2 s-1, 12:12 (light:dark) 주기의 조건으로 15일에 한번 씩 순차 배양 (serial transfer) 되었으며, 규조류와 와편모조류의 경우 DM (Beakes et al. 1988) 배지, 15˚C, 30-40 μmol m-2 s-1, 12:12 (light:dark) 주기의 조건으로 20일에 한번 씩 순차 배양되었다.
2.3 최우수 살조물질 선정을 위한 살조효과 평가
조류 대발생 수준의 남조 D. flos-aquae와 M. aeruginosa (1 × 106 cells mL-1) 배양액 0.2 mL을 96 well plate (SPL)에 분주 후, 합성된 92 종의 화합물을 1, 5, 10, 20, 50 μM 농도로 각각 접종하였다. NQ 살조물질이 접종된 well plate는 20˚C, 30-40 μmol m-2 s-1, 12:12 (light:dark) 주기 조건의 배양기에서 10 일간 배양되었으며, 접종 당일, 접종 후 1, 3, 5, 7, 10 일차 세포를 계수하였다. 조류에 대한 살조효과를 평가하기 위해 광학 현미경 (Olympus IX71, Japan)의 200-400 배에서 Sedgwick-Rafter chamber (PhytoTech Inc., USA)를 이용해 계수하여 대조구 대비 살조활성 (algicidal activity)을 평가하였다. 살조활성은 microplate assay 실험 후 계수한 결과를 이용하여 다음 (Eq. 1)과 같은 식으로 계산하였다.
살조활성 (Algicidal activity) (%) = (1 – T / C) × 100 (Eq. 1)
상기 식에서 C는 화합물을 접종하지 않은 대조구의 세포 수, T는 물질 접종 7 일 후 세포 수를 의미한다. Microplate assay 결과를 이용하여 높은 살조 활성을 나타낸 살조물질을 최우수 물질로 선정하였다.
2.4 최우수 살조물질의 살조 범위 및 최적 농도 선정
유해 남조류 D. flos-aquae와 M. aeruginosa에 대하여 microplate assay 실험을 통한 결과를 바탕으로 선정된 최적 살조물질의 남조류 선택적 제어의 가능성을 평가하기 위해 규조류 및 와편모조류에 대해 microplate assay를 진행하였다. 규조 C. meneghiniana, S. hantzschii, 와편모조류 P. bipes 세포를 각 5 × 105 cell mL-1로 준비하여, 48 well plate에 최종 선정된 화합물을 1, 5, 10, 20 50 μM의 농도로 접종하였다. 접종 후 규조류와 와편모조류는 15˚C, 40 μmol m-2 s-1, 12:12 (light:dark) 주기 조건의 배양기에서 10일간 배양되었다. 세포의 계수는 남조류 microplate assay 실험과 동일하게 진행되었다. 또한, 현장 적용을 위한 최적 농도를 찾기 위해서 NQ 화합물 접종 240 시간 경과 후 상기조류 세포수를 50% 제어할 수 있는 농도 (IC50-240 h)를 standard curve인 four Parameter logistic curve (Findlay and Dillard 2007)를 사용해 Sigmaplot version 10 software (Systat Software Inc., USA)에서 계산하였다 (Eq. 2).
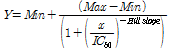 (Eq. 2)
(Eq. 2)
Y는 화합물 각각의 접종농도에 따른 살조활성 (%)을 나타내며, Max는 접종농도에 따른 최대 살조활성 (%), Min는 접종농도에 따른 최소 살조활성 (%), X는 접종농도 범위 내의 IC50-240 h 값, - Hill slope (- 기울기) 값을 의미한다. 따라서 상기 식을 사용해 접종농도 별 살조 활성의 IC50 값을 구하였다.
2.5 생태독성 평가
2.5.1 급성 독성평가
조류 생태독성 평가 시험 (eco-toxicity test)은 Selenastrum capricornutum (CCAP, United Kingdom)을 분양 받아 시험하였다. 대수성장기의 S. capricornutum 1 × 104 cells mL-1을 실험 시작밀도로 NQ 40 물질을 농도 별 (0, 0.1, 0.2, 0.5, 1.25, 2.5, 5, 10, 20 μM)로 접종하여 실험을 수행하였다. 혼합 배양액은 axenic 상태의 지표생물 최적성장 조건으로 배양되었다 (20˚C, 50 μmol photons m-2 s-1, EG:JM medium, 12:12 (light:dark) 주기 조건). 세포의 계수를 위해 24시간 간격으로 72시간 동안 Sedgwick-Rafter counting chamber (PhytoTech Inc., USA)를 사용하여 ×200 배율의 광학현미경 (Zeiss Axioplan, Germany) 하에서 계수하였다. 실험은 3번 반복하여 실험하였다 (OECD 2011).
동물플랑크톤의 급성독성시험은 생태독성 지표생물인 담수산 물벼룩 Daphnia magna를 시험에 사용하였다. 시험용 D. magna의 사육은 2009년 10월 국립환경과학원으로부터 분양 받아 한양대학교 물환경생태복원 연구실에서 지속적으로 배양하여 시험에 사용하였다. 배양 조건은 수온 20 ± 1˚C, 광도 50 µmol photons m-2 s-1, 12:12 (light:dark) 주기 조건으로 U.S. Environmental Protection Agency guideline에서 제시한 moderately hard water (MHW)를 제조하여 24시간 동안 폭기시킨 뒤 사용하였다. D. magna의 먹이로는 녹조류인 S. capricornutum 또는 Chlorella vulgaris를 공급하였다. 급성독성 시험에 사용된 D. magna 는 3회 이상 어린 개체를 생산한 산란용 어미로부터 얻은 개체 가운데 생후 24일 미만의 어린 개체만을 선별하여 시험을 수행하였다. 대조구 (0 μM 살조후보 물질)과 공비를 2로 하여 희석한 농도 (0, 0.1, 0.2, 0.5, 1.25, 2.5, 5, 10 및 20 μM)로 접종하였으며, 48시간 동안 노출시켰다. 노출 기간 동안에는 먹이를 공급하지 않았으며, 각 농도별로 4개의 반복실험구로 시험하였다. 각각 배양수 75 mL에 D. magna 5마리씩 넣어 총 180마리를 사용하였다. 실험조건은 배양조건과 동일하게 12:12 (light:dark) 주기, 온도는 20 ± 1˚C로 유지하였다. 시험을 시작하기 전과 종료 후에 농도 별 실험수의 온도, pH, DO를 측정하였고, 종말점 (endpoint)은 24, 48 시간 후 실험구와 D. magna 자극 후 15초 후에 관찰하여 일부기간 (촉각, 후복부 등)만 움직이나 유영할 수 없는 유영저해 (immobilization)와 사망 (lethality)을 육안으로 관찰하여 판단하였다 (OECD 2004).
어류 zebrafish (Danio rerio) 급성독성시험에 사용된 zebrafish는 구입 (Sejin Aquarium Co., Seoul, South Korea)하여 실험을 수행하였다. 유리수조의 유수식 배양 시스템을 이용하여 5와 20 L로 각각 나누어 25 ± 1˚C, pH 7.5 ± 0.2, 용존산소 7-8 mg L-1 및 광주기 12:12 (light:dark) 주기 조건으로 사육하였으며, 먹이로 매일 Tetramin를 공급하였다. 사육수는 수돗물을 일반 필터로 1차 여과한 후, 탄소 필터로 2차 여과하여 활성탄으로 탈염하여 사용하였다. 부화 후 3개월 이상 된 2 ± 1 cm 크기의 개체를 이틀간 절식시킨 후 시험을 수행하였다. 시험 시작 전 14일 동안 0%의 사망률을 확인하고 순응시킨 뒤, zebrafish (D. rerio)를 선별하여 준비하고 최종 선정된 물질을 농도 별로 접종하여 각각 0, 0.1, 0.2, 0.5, 1.25, 2.5, 5, 10 및 20 μM이 되도록 준비하였다. 시험 기간 동안에는 시험액을 교환하지 않는 지수식 시험방법 (static non-renewal test)으로 진행하였으며, 또한 시험기간 동안에는 먹이를 공급하지 않았다. 시험 조건으로는 최적 배양조건과 동일하게 설정하여 수행하였다. 24시간 간격으로 96시간 동안 지표생물 사망률과 기형율 변화를 관찰하였다 (OECD 1992).
2.5.2 D. magna를 이용한 만성 독성평가
D. magna의 급성 독성 평가를 통해 얻어진 결과를 바탕으로 최종 선정된 NQ 물질을 장기간 노출 시켰을때 물벼룩 D. magna의 생존, 성장, 번식 등에 미치는 영향을 평가하였다. 시험에 사용한 물벼룩 D. magna는 모두 24시간 이전에 출산한 건강한 어린 개체를 사용하였고 시험에 사용한 시험용수는 급성독성 평가와 같다. 시험기간은 시험 물벼룩의 평균수명을 고려하여 21일간 조사하였다 (OECD 1996). 물질의 농도를 일정 수준으로 유지시키기 위해 2일에 한번씩 NQ 물질을 처리한 사육수로 교체하였다. 시험 조건은 급성독성 평가 시와 동일하였고 시험 물벼룩 D. magna의 수는 각 처리당 10마리를 개별적으로 75 mL의 배양수에 투입하였고, 먹이는 S. capricornutum을 2.5-5 × 105 cells mL-1의 농도가 되게 공급하였다. 최종 선정된 NQ 물질의 농도는 0.1, 1, 10 µM 세개의 농도와 배양액만을 담은 대조구와 함께 시험을 수행하였다. 21일 동안 생존여부, 성장을 위한 탈피 횟수, 번식능, 유영저해 등을 매일 관찰하였고, 번식된 어린 물벼룩은 계수 후 시험용기에서 제외시켰다. 시험 최종일에는 어미 물벼룩의 몸길이를 측정하여, 최종 성장에 관하여 대조구와 비교 분석하였다. 몸길이의 유의적 차이 분석을 위한 통계처리는 일원 분산분석 (one-way ANOVA)을 실시하였다 (p<0.05).
3. 결 과
3.1 남조류 제어 가능한 화합물 선정을 위한 살조효과 평가
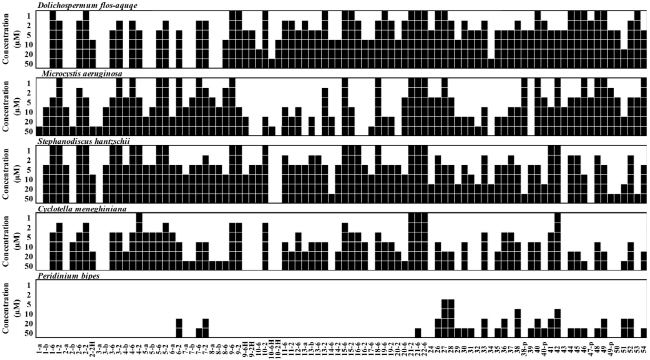
Naphtoquinone 화학구조를 기반으로 한 합성물질을 이용하여 유해 남조류 Microcystis, Dolichospermum 종을 대상으로 살조효과를 평가하였다. 조류 대발생 수준의 남조류 D. flos-aquae와 M. aeruginosa (1 × 106 cells mL-1)에 합성된 화합물을 92종에 대하여 1, 2, 5, 10, 20, 50 μM의 다양한 농도로 microplate assay를 진행하여 살조효과를 평가한 결과, D. flos-aquae의 경우, 총 22개의 물질 (1-2, 3-2, 4-6, 5-6, 5-2, 6-2, 7-6, 9-6, 10-6H, 15-6, 18-6, 21-2, 21-6, 22-6, 27, 38-p, 40, 42, 45, 48, 49, 54) 1 µM 농도에서 80% 이상의 살조효과를 나타내었다. 또한, M. aeruginosa의 경우에서도, 총 22개의 물질 (1-6, 2-2 9-6, 9-2, 9-6H, 10-2, 13-2, 15-6, 15-2, 19-6, 21-2, 21-6, 22-6, 26, 27, 40, 44, 45, 46, 48, 49, 53) 1 µM 농도에서 80% 이상의 살조효과를 나타내었다 (Fig. 2). 앞서 기재한 22개 물질 이외의 다른 합성물질의 경우 대부분 50, 20 µM의 고농도에서는 80% 이상의 살조효과를 나타내었으나, 5, 2, 1 µM의 농도에서는 살조효과가 낮게 (<80%) 관찰되었다. Micro-plate assay 살조효과 결과를 바탕으로 D. flos-aquae와 M. aeruginosa에 대한 물질의 IC50 값을 도출한 결과, 92개의 물질 중 8개 물질 (2-2. 15-2, 19-6, 21-2, 21-6, 22-6, 40, 46)이 D. flos-aquae에 대하여 낮은 IC50 (<0.5 µM) 값을 보였으며 (Table 1), M. aeruginosa는 5개 물질 (1-2, 6-2, 21-2, 40, 49)이 낮은 IC50 (<0.5 µM) 값을 보였다 (Table 2). 최우수 살조활성을 보유한 살조물질 중에서 IC50-240 h 값 만을 비교했을 때, M. aeruginosa와 D. flos-aquae 제어를 위한 최적 살조물질은 각기 달랐으나, M. aeruginosa와 D. flos-aquae를 공통적으로 제어하기 위해서는 NQ 40이 가장 적합할 것으로 사료되었다.
3.2 살조물질의 살조 범위 및 최적 적용 농도 평가
최적 살조물질로 선정된 NQ 40 물질의 살조 범위를 평가하기 위해 규조류 S. hantzschii, C. meneghinia, 와편모조류 P. bipes에 대하여 microplate assay를 수행하여 평가하였다. 그 결과, 규조류 S. hantzschii, C. meneghinia에 대해서는 합성된 대부분의 물질이 50, 20, 10, 5 µM의 고농도에서는 80% 이상의 살조효과를 나타내었으나, 2, 1 µM의 낮은 농도에서는 살조효과가 현저히 낮게 (<80%) 관찰되었다. 와편모조류 P. bipes의 경우, 1-a 부터 22-6까지는 80% 이상의 제어 효과를 갖는 물질이 거의 없었으며, 26부터 54번까지 물질 중에도 5 µM의 농도에서는 80%이상 살조효과를 갖는 물질도 2개 (NQ 27, 28)만 관찰되었다 (Fig. 2).
최종 선정된 NQ 40 물질의 1 µM 농도에서 M. aeruginosa, D. flos-aquae는 99.6%, 100%의 살조효과를 보였으나, S. hantzschii에 대해서는 34.3%, C. meneghinia, P. bipes 두 종에 대해서는 오히려 세포가 증진되는 결과를 관찰하였다 (Table 3). 앞선 결과를 바탕으로 IC50 값을 도출한 결과, D. flos-aquae, M. aeruginosa, S. hantzschii, C. meneghinia, P. bipes 대하여 각각 0.37, 0.16, 1.7, 6.2, 13.1 µM으로 측정되었다 (Table 3). 즉, 선정된 최적 살조물질 NQ 40은, S. hantzschii, C. meneghinia, P. bipes 종에 2, 1 µM에서는 살조효과가 관찰되지 않았다. 따라서, 남조류 제어를 위하여 최종 선정된 살조물질 NQ 40 물질은 남조류 M. aeruginosa, D. flos-aquae 종에 선택적으로 우수한 살조활성을 갖는 것으로 확인되었다. 또한, 현장에서 유해 남조류 M. aeruginosa, D. flos-aquae 을 제어하기 위해 NQ 40 물질을 적용한다면 1 µM 농도가 적합할 것으로 사료되었다.
3.3 생태독성 실험
3.3.1 급성 생태독성 평가
실제 수계에 노출되었을 경우 수생태계에서 생산자와 소비자 역할을 하는 조류, 물벼룩, 어류에 대하여 각각 어떠한 영향을 미치는지 알아보고자 생태독성 지표생물을 이용하여 실험을 수행하였다. S. capricornutum, D. magna, D. renio을 이용한 생태독성 실험은 총 9개 (0, 0.1, 0.2, 0.5, 1.25, 2.5, 5, 10 및 20 μM)의 농도로 접종하여 72, 48, 96시간 동안 성장률, 사망률, 유영저해를 관찰하였다. 그 결과, S. capricornutum, D. magna, D. renio 모든 생물군에서 NQ 40물질의 최적 사용농도인 0.5-1 μM 에서는 독성이 관찰되지 않았다. 각 생물에 대하여 EC50/LC50값을 도출한 결과, S. capricornutum (3.20 μM), D. magna (14.5 μM), D. renio (15.7 μM)로 측정되었다 (Table 4). 따라서, 지표생물 S. capricornutum, D. magna, D. renio를 이용한 NQ 40 물질의 생태독성 실험 결과 최적 적용 농도에서 급성독성은 없는 것으로 판단하였다.
3.3.2 만성 생태독성 평가
Table 5의 결과는 NQ 40 물질의 장기간 노출시 미치는 영향을 평가하기 위해 D. magna를 NQ 40 물질에 21일간 노출시켰을 때 생존율 (survival rate), 성장 (growth), 번식 (reproduction)에 미치는 영향을 나타낸 것이다. 21일동안 0.1, 10 μM 농도의 NQ 40 물질 처리구에서 생존율 (survival rate)은 100% 였으며, 1 μM 농도의 처리구에서만 19일째 90%로 감소하였다. 생존한 어미개체로부터 첫 출산 (first day of reproduction)까지 걸리는 시간은 대조구와 1 μM에서는 7일, 0.1, 10 μM 농도에서는 8일로 관찰되었으며, 21일간 출산한 새끼 물벼룩의 누적 개체수 (accumulative reproduction)는 대조구에서는 505 개체, 0.1, 1, 10 μM 농도에서는 각각 509, 454, 385 개체로 관찰되었다. 또한, D. magna의 성장을 위한 필요한 탈피는 2-3일 간격으로 지속적으로 관찰되었고, 21일 동안 탈피 누적 횟수 (accumulative moltings)는 대조구, 0.1, 1, 10 μM 농도에서 각각 82, 87, 77, 79회를 관찰되었다. 최종 성장에 대하여 관찰하기 위해 21일 실험 종료 후 어미개체의 몸길이 (body length)를 측정하였다 (CellSens program, Olympus America, Center Valley, PA). 그 결과, 대조구 (3.91 ± 0.12 mm), 0.1 μM (3.88 ± 0.25 mm), 1 μM (4.03 ± 0.11 mm), 10 μM (3.87 ± 0.25 mm)로 측정되었으며, 유의적인 차이는 없었다 (Table 5).
4. 고 찰
유해 조류를 제어하기 위해 개발된 기존 조류제어 물질의 경우, 대부분 비선택적인 넓은 살조 범위로 인하여 수생 생물에 영향을 주어 결국 수중 생태계를 파괴할 수 있는 문제점이 발생하였다 (Koss and Snyder 2005, Gumbo et al. 2010). 따라서, 최근에는 생태계 교란을 최소화 하기 위해 자연계 존재 혹은 생물로부터 유래한 물질을 이용한 조류 제어기술의 개발이 이루어 지고 있다 (Yamamoto et al. 1998, Nakai et al. 2000, Nakai et al. 2005, Shao et al. 2011, Wu et al. 2011). 본 연구에서 사용된 NQ 물질 역시 자연계 식물 (Diospyros ebenum, Impatiens balsamina etc.) 및 미생물 (Streptococcus faecalis etc.) 내 존재하는 천연물로서, 다양한 기능을 갖고 있어 의약품 (medical supplies), 제초제 (herbicide), 살균제 (antimicrobial agent) (O’Brien 1991, Monks et al. 1992, Schrader et al. 2003, Dong et al. 2009, Menna-Baretto et al. 2009) 등 여러 방면에서 사용되고 있다. 또한, 자연상태에서 산화-환원 반응을 조절하는 물질로 쓰이며 (Harn et al. 2010), 비타민 K와 유사한 구조를 갖는다는 성질을 점을 착안하여 새로운 녹조제어 물질로 선택하였다 (Combs 1976). 또한, NQ 계열 물질은 식물의 광합성 체계를 교란하여 광합성 작용을 교란한다는 보고가 있다 (Biggins et al. 1990, Jewess et al. 2002). 따라서, 본 연구에서는 실제 녹조 현장에 적용하기 위한 기법으로, 기존의 NQ 유도체 (1,4- naphthoquinone과 9,10-anthraquinone 등)와는 다르게 골격구조 변화로 신규 유도체를 합성하여 담수 유해 남조류인 Microcystis, Dolichospermum에 대한 살조효과를 입증하고자 하였다.
본 연구에서는 기존 살조물질의 비선택적인 조류 제어 문제점을 보완하고자 국내에서 빈번하게 출현하여 피해를 유발하는 유해 남조류 2종을 제외한, 규조류 2종 S. hantzschii, C. meneghinia, 와편모조류 1종 P. bipes에 대하여 추가적으로 NQ 물질의 살조효과를 평가하였다. 최종 선정된 NQ 40 물질은 D. flos-aquae, M. aeruginosa, S. hantzschii, C. meneghinia, P. bipes 각 조류에 대하여 0.37, 0.16, 1.7, 6.2 및 13.1 µM의 IC50 값을 나타내었다. 제어하고자 하는 남조류의 경우, 규조류 및 와편모조류 보다 낮은 IC50 값을 나타냈으며, 이러한 결과는 NQ 40 물질이 기존 살조물질의 문제점인 비선택적 제어효과가 보완된 유해 남조류에 대해서 선택적인 제어가 가능한 살조물질로 보다 친환경적으로 사용될 수 있을 것으로 사료된다.
생태독성 평가란, 특정 물질의 유입 및 노출이 생태계에 미치는 영향을 연구하는 것이며, 생태계로 유입된 독성 물질은 무기적 환경조건과 생물 군집 구조에 따라 직접적으로, 또는 먹이사슬을 통한 간접적인 방법으로 생물체내에 유입된다. 이는 작게는 개체의 정상적인 생존에 영향을 주지만 크게는 생태계 전체의 균형을 파괴하는 결과로 이어지게 된다. 따라서 생태독성 평가를 위해서는 생태계를 구성하는 다양한 생물상을 대상으로 하는 것이 바람직하며 수생태계의 먹이망을 고려하여 수행하여야 한다. 이는 단일 물질이나 수계 시료의 독성을 종합적으로 판단 할 수 있게 한다. 즉, 본 연구에서는 녹조제어를 위한 NQ 물질이 현장 적용 시 생태계의 미치는 독성 정도를 평가하기 위해서 EPA와 OECD에서 선정된 생태독성 평가 지표생물을 통한 생태독성 평가를 진행하였다. 수 생태계의 주요 영양 단계 중 가장 하위단계를 차지하는 기초 생산자 조류는 상위 영양 단계의 먹이로 제공되기 때문에 먹이 사슬에서 중요한 역할을 하는 생물이다. 또한 물벼룩 (D. magna)은 호소생태계에서 식물플랑크톤을 섭식하는 미세초식자로서 생물 생산 및 물질 순환 과정에서 중요한 역할을 하며, 화학물질에 매우 민감하여 생태독성 시험의 대표적인 지표생물이다. Zebrafish (D. rerio)는 우리나라를 비롯하여 전세계적으로 분포하며 국제적으로 신뢰성 있는 표준시험법의 공시어종으로 생태독성평가에 널리 사용되는 생물종이다. 본 실험에서는 미세조류 (S. capricornutum), 물벼룩 (D. magna), 어류 (zebrafish)를 대상으로 급성생태독성을 평가하여 생태계 내 미치는 영향을 평가하기 위한 목적으로 실험을 수행하였다. 남조류 제어를 위해 최종 선정된 살조물질 NQ 40의 경우, 미세조류 S. capricornutum 에 대한 EC50 값은 3.20 μM (1.031 mg/L), 동물플랑크톤 D. magna에 대한 EC50 값은 14.5 μM (4.669 mg/L), 어류 D. renio에 대한 LC50 값은 15.7 μM (5.055 mg/L)으로 측정되었다. 기존에 개발되어 사용되고 있는 CuSO4, Triclosan 등의 살조물질과 비교해보면, CuSO4는 S. capricornutum, D. similis, D.rerio에 대한 EC50/LC50값은 0.344, 0.032, 0.094 mg/L으로 보고되었다 (De Oliveira-Filho et al. 2004). 또한, Triclosan 물질의 경우, S. capricornutum, D. magna, D.rerio에 대한 EC50/LC50값은 0.0047, 0.39, 0.42 mg/L으로 보고되었다 (Orvos et al. 2002, Tatarazako et al. 2003, Oliveira et al. 2009). 이러한 결과는 기존에 개발되어 유해 녹조 제어를 위해 사용되고 있는 살조물질에 비해 낮은 독성을 갖는다는 것을 의미하며, 보다 친환경적으로 현장에서 사용이 가능할 것으로 판단된다. 더불어, 본 연구에서는 급성 독성 평가뿐만 아니라, NQ 40 물질이 실제 수계 적용 후 물질의 잔류에 의한 장기간 노출 시 미치는 영향을 평가하고자 D. magna를 이용한 만성 독성 평가를 수행하였다. 현장 적용시 최적 농도인 0.5-1 µM을 고려하여 0.1, 1, 10 µM로 21일동안 지속적으로 노출 후 생존율 (survival rate), 성장 (growth), 번식 (reproduction)에 관하여 관찰한 결과, NQ 40 물질을 처리하지 않은 대조구 대비 생존에 대한 독성은 관찰되지 않았다. 또한, 성장을 위한 탈피 횟수, 최종 성장 후 몸의 길이 측정 결과 대조구 대비 유의적인 차이가 없었다. 하지만, 21일동안 D. magna의 어미성체로부터 번식한 개체수를 비교 분석한 결과, 대조구, 0.1, 1, 10 µM 실험구 각각 505, 509, 454, 385 개체수를 번식하였다 (Table 5). 접종 최고 농도인 10 µM 농도에서는 다소 낮은 개체수를 번식한 것으로 보아 수계 내 NQ 40 물질이 고농도로 장기간 노출 시 번식에 독성을 나타낼 수 도 있다고 판단하였다. 하지만, NQ 40 물질의 현장 적용을 위한 최적 농도는 0.5-1 µM 농도이기 때문에 수계 적용한다면 수생생물에 독성은 없을 것으로 사료된다.
본 연구를 통해서 개발된 NQ 살조물질에 대한 선택적인 살조기작에 대한 연구는 이번 연구에서 수행되지 않았지만, 몇가지 주요 요인을 추측할 수 있다. 먼저, 식물플랑크톤의 형태, 크기, 세포 내 구조 (subcellular structure), 생화학적 조성 (biochemical composition), 화학물질에 대한 민감성 (susceptibility) 등이 NQ 물질이 세포 내 독성으로 작용하는 하는 요인이 될 것이다 (Jori and Brown 2004). 또한, NQ 유도체의 화학구조 (기본 골격 구조의 형태, 다양한 치환기의 형태, 수, 위치, 화합물의 charge)에 의해 작용할 가능성이 있다 (Segalla et al. 2002). 이러한 화학구조에 의한 살조효과 변화에 대하여 규명을 위해서는 추후 살조활성과 화학구조식에 대한 상관관계 분석이 필요하다. 마지막으로 중요한 요인은 NQ 40 물질 적용시 환경에서의 빛의 강도와 파장이다 (Jančula et al. 2008). 높은 강도의 빛은 singlet oxygen의 생산율과 매우 밀접한 관계를 갖고, 이러한 singlet oxygen은 ROS (reactive oxygen species) 생성과도 연관이 있기 때문에 상대적으로 더 높은 독성효과를 나타낼 수 있다. 많은 연구를 통해서, 다양한 quinone 구조의 화합물들이 세균, 바이러스, 효모, 곰팡이 등에게 우수한 세포독성을 보였으며, 특히 남조류와 매우 유사한 특징을 가지고 있는 세균 등에 작용하는 주요기작이 free radical에 의한 superoxide의 생성이었다 (Bertoloni et al. 1992). 그 외에도 NQ의 구조를 갖고 있는 약물들은 DNA 복제에 관여하는 topoisomerase에 작용하여 세포분열 억제효과를 나타내는 것으로 알려져 있다. 그러나 본 연구에서는 singlet oxygen의 생성 및 다양한 기작에 대한 연구를 수행하지 않았다. 따라서, NQ 물질의 정확한 살조기작에 대한 연구는 추후 반드시 수행되어야 하며, 선택적 살조효과에 대한 기작이 규명된다면 보다 효과적이며 친환경적인 살조물질로서 사용이 가능하게 될 것이다.
5. 결 론
여름철 유해 조류 대발생에 의한 피해를 막고자 개발된 NQ 40 물질은 1 µM 농도에서 대상 종인 D. flos-aquae와 M. aeruginosa에 높은 살조효과 (100%, 99.6%)를 나타냈다. 하지만, 대상 종 이외의, S. hantzschii, C. meneghinia, P. bipes 종에는 최적 적용 농도 1 µM에서 살조효과가 관찰되지 않았다. 더불어, 지표생물을 이용한 급성, 만성 생태독성 평가 결과, 최적 적용 농도 1 µM에서는 급성 및 만성 독성이 관찰되지 않았다. 따라서, 본 연구를 통해 개발된 생물유래 합성물질 NQ 40은 D. flos-aquae와 M. aeruginosa 종에 대하여 선택적으로 제어가 가능하며, 수생생물에 독성이 없는 물질로서 친환경적인 녹조제어 물질로 사용 될 수 있을 것이다.