1. 서 론
2. 재료 및 방법
2.1 Naphthoquinone 유도체 (NQ 2-0: 2-((2- (Diethylamino)ethyl)amino)naphthalene-1, 4-dione)
2.2 Mesocosm (30 ton) 내 Naphthoquinone 2-0 (NQ 2-0)의 적용
2.3 Mesocosm에서 비생물학적 요인 모니터링
2.4 Mesocosm에서 생물학적 요인 모니터링
2.5 Mesocosm (30 ton) 내 식물플랑크톤 종 다양성 분석
2.6 데이터 분석
3. 결 과
3.1 Naphthoquinone 2-0 (NQ 2-0) 물질의 선택적 살조효과
3.2 Naphthoquinone 2-0 (NQ 2-0)의 mesocosm 내 적용 후 모니터링
3.2.1 비생물학적 요인의 변화
3.2.2 생물학적 요인의 변화
4. 고 찰
1. 서 론
여름철 남조류에 의한 녹조 대발생은 상수원 수원지를 포함한 하천 생태계 훼손 및 정수 비용 증가 등의 피해가 발생할 뿐만 아니라 경제적, 공중보건 측면에서 심각한 문제를 야기시킨다. 특히, Microcystis sp. 종과 같은 유해 남조류는 미관상의 불쾌감, 음용수의 이취미 발생으로 인한 먹는물 확보에 어려움을 줄뿐만 아니라, 간독소 microcystins을 생성하여 야생 동물과 가축에 치명적인 해를 주며, 인간의 건강까지 위협한다 (Kiviranta et al. 1991, Oberholster 2004, Kang et al. 2012).
유해 조류 제어를 위해 생물학적, 물리, 화학적 제어 방법 등의 다방면에서 친환경적인 제어 방법이 개발되었으나 (Ahn et al. 2003, Jeong et al. 2008, Kang et al. 2005, Kang et al. 2007, Kang et al. 2011), 실험실 내의 높은 살조효과를 바탕으로 현장 적용하여 성공적인 유해 조류 제어효과를 보인 기술도 매우 적으며, 수생 생물에 대한 영향, 설치 및 운영비용, 녹조제어 효율성의 변동, 대량생산 등의 다양한 문제점으로 인해 지속적인 기술 개발이 요구되고 있는 실정이다. 따라서, 최근에는 앞선 단점을 보완하기 위해 생물유래 물질을 이용한 녹조 제어 물질 개발이 이루어 지고 있다 (Nakai et al. 2005, Shao et al. 2011, Wu et al. 2011). 본 연구진은 다양한 식물 (cf. Droseraceae, Juglandaceae, Nepenthaceae, Plumbaginaceae)과 미생물 (Streptococcus faecalis)에서 생성 혹은 자연계 존재하는 naphthoquinone (O’Brien 1991, Monks et al. 1992, Tangmouo et al. 2006, Rahmoun et al. 2012)을 기반으로 유해 조류에 선택적이며, 저독성의 녹조제어 물질을 개발하였다 (Byun et al. 2015, Joo et al. 2016b). 더불어, 경제적인 현장 적용을 위하여 물질의 개량 연구를 통해 합성단계를 최적화하였으며, 최적화된 물질의 선택적 살조효과 및 저독성을 입증하였다 (Joo et al. 2017). 그러나, 최종 선정된 물질은 현장 조건에서의 살조효과와 다른 생물학적 요인과 비생물학적 요인에 대한 평가는 이루어 지지 않았다. 따라서 본 연구에서는 최종 선정된 물질의 현장 적용 가능성을 평가하기 위해 mesocosm 실험을 통해 확인하고자 하였다. 수 생태계 연구에 유용한 도구로서 다양한 분야에 이용되는 mesocosm 실험은 실제 현장에서 자연 생태계 시스템의 기능과 구조를 단순화 시킨 생태계 실험의 방법이다. 더구나 현장수를 이용한 mesocosm 실험은 화학적인 교란 혹은 새로운 환경조건 (수온 상승, CO2 농도 증가, 새로운 화학물질 등)이 수 생태계에 작용되었을 때 생태계 반응을 평가하기 좋은 방법이며 (Ahn et al. 2001, Naito et al. 2003, Orihel et al. 2006) 더구나, 유해 조류가 발생한 현장수를 이용한 mesocosm 실험은 실험실에서 확인된 살조물질의 효과를 현장 유사 생태계 내에서 검증하고, 적용 시 발생할 수 있는 살조효과 및 독성에 의한 생태계 교란에 대한 요인들을 현장 적용 이전에 미리 확인할 수 있기 때문에 (Odum and Odum 2003, Willis et al. 2004) 실험실 내 연구결과와 실제 현장적용 사이의 차이를 줄일 수 있는 중요한 실험이다 (Han et al. 1995, Wirth et al. 2004). 따라서, 개발된 살조물질의 mesocosm 실험은 실험실 내의 소규모 실험이 아닌 큰 규모 실험에서의 살조효과 분석 및 새로운 물질의 생태계 적용 시 발생 가능한 문제점의 확인을 위한 목적으로 수행되었다.
본 연구에서는 생물유래 물질인 naphthoquinone (NQ) 2-0 물질을 현장 적용에 앞서 mesocosm 적용하여 현장 Microcystis 종에 대한 살조효과 평가뿐만 아니라, 식물플랑크톤 군집을 포함한 수계 내 다양한 생물의 변화와 다양한 비생물학적 요인의 모니터링을 통하여 개발된 살조물질의 현장 적용 가능성을 평가하고자 하였다.
2. 재료 및 방법
2.1 Naphthoquinone 유도체 (NQ 2-0: 2-((2- (Diethylamino)ethyl)amino)naphthalene-1,4-dione)
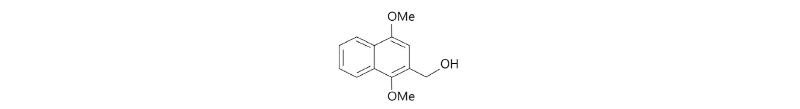
Naphthoquinone 유도체 (NQ 2-0)의 모체가 되는 기본적인 화학적 구조는 Fig. 1에 표시하였다. 모체를 기반으로 상온에서 교반된 naphthalen-1,4-dione 158 mg에 메탄올 5 mL를 이용하여 화합물을 제조하였다. 구체적으로, 상온에서 반응 24 시간 후, 반응혼합물을 진공에서 농축시키고, flash column chromatography (100% EtOAc)에 의해 정제하여 화합물을 수득하였다. 합성된 유도체의 구조적 결정과 정제를 위해 1H NMR (Varian Mercury 400 MHz, Varian Inc., Palo Alto, CA, USA)과 HPLC (high performance liquid chromatography)를 이용하였으며, 유도체의 분자량 측정을 위해 GC/MS (gas chromatography–mass spectrometry)를 이용하였다. 본 실험에 사용한 naphthoquinone 유도체는 한양대학교 화학과 조천규 교수팀 연구실에서 합성하여 제공받았다.
2.2 Mesocosm (30 ton) 내 Naphthoquinone 2-0 (NQ 2-0)의 적용
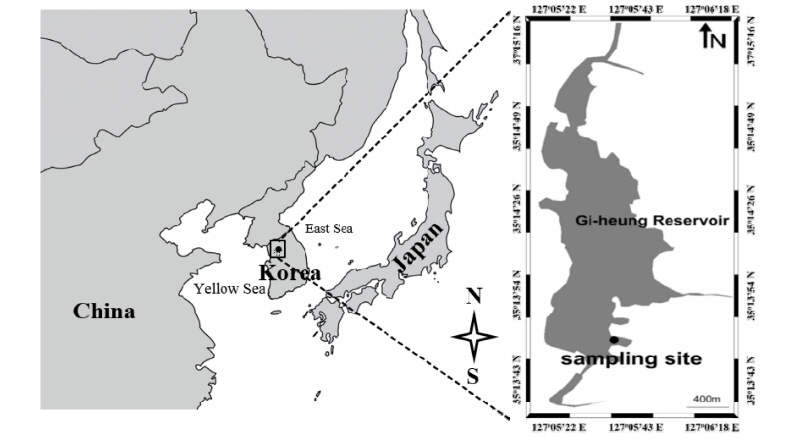
실험실 내 실험에서 우수한 살조효과가 입증된 NQ 2-0 물질의 현장 적용 가능성과 생태계 미치는 영향을 평가하기 위해 mesocosm 내 접종 후 현장에 존재하는 남조류 Microcystis sp. 제어효과 및 생물학적, 비생물학적 요인을 모니터링 하고자 하였다. Mesocosm의 경우, 매년 여름철 남조류 Microcystis sp. 종에 의한 녹조 대발생에 의해 문제가 발생하는 기흥저수지 수변 (경기도 용인시 기흥구 지역: 37°14'56.8"N, 127°05'28.6"E)에 2014년 9월 실험구를 설치하여 수행하였다 (Fig. 2). 선정된 지역 내 부지에 미국 Pastel 사의 30 ton (6 m3×7 m3×1.5 m3) 규모의 직사각형 실험구 2개 (대조구, NQ 2-0 처리구)를 설치하였고, 기흥저수지 내 남조류가 조류 경보수준으로 존재하는 현장수를 수중 펌프를 사용하여 채수하여 2일간 실험구를 안정화 한 후 물질을 접종하였다. NQ 2-0 물질의 mesocosm 적용 후 수 생태계에 미치는 영향을 평가하기 위해 매일 11:00- 13:00의 동일한 시간에 채수하여 다양한 물리・화학적・생물 요인들을 분석하였다.
2.3 Mesocosm에서 비생물학적 요인 모니터링
수온, pH, 용존 산소 (dissolved oxygen, DO), 전기전도도 (conductivity), 탁도 (turbidity) 등은 U-10 수질측정기 (water quality meter) (HORIBA, Japan)를 이용하여 측정하였으며, 용존 산소의 경우 Winkler titrator로 추가 검증하였다. 또한, mesocosm 실험은 샘플링에 앞서 각각의 실험구에 PVC pipe를 사용하여 수층을 잘 혼합시켜 바닥에 가라앉은 (bottom-dwelling) 미생물들을 부유 시켜 주었다. 샘플은 접종 당일, 2, 4, 6, 8, 10, 15일차까지 각 실험구의 표층수에서 1 L의 폴리에틸렌 병으로 채수하였다. 염양염 (nitrite: NO2-N, nitrate: NO3-N, ammonium: NH4-N: phosphate: PO4-P, silicate: SiO2-Si) 분석을 위해 250 mL을 실험구와 대조구에서 각각 채수하여 glass fiber filter (GF/F) (Whatman Inter-national, Maidstone, UK)로 여과한 후 산처리된 poly-ethylene bottle에 50 mL씩 나누어 -70°C deep freezer에 보존하였다. 모든 영양염 분석은 APHA (2005)에 의거하여 각각 분석하였다.
2.4 Mesocosm에서 생물학적 요인 모니터링
박테리아 (bacteria), 종속영양 미소편모류 (heterotrophic nanoflagellates, HNFs), 식물플랑크톤 (phytoplankton)의 세포수를 계수하기 위해 샘플 1 L를 채수하고 산 처리된 300 mL의 polyethylene bottle에 담아 glutaraldehyde (final concentration 2%)로 고정하여 4°C에서 암소 보관하였다.
박테리아와 HNFs의 경우, 각각 2 mL, 10 mL을 분취하고 아래와 같은 방법으로 직접 계수해주었다 (Riemann et al. 1990). 각각의 샘플은 DAPI (5 µg mL-1 final con-centration)로 5 분간 염색한 후, black 0.2-µm-pore-size polycarbonate filters (poretics) 하에서 포집하고 1,000 배율 (magnification)의 Zeiss Axioplan epifluorescence microscope 하에서 백색으로 발광하는 세포를 계수하였다. 대략, > 200 cells filter-1 (또는 > 10 fields filter-1)의 세포수를 계수하였다. Nanoflagellates의 경우 flagellate 크기를 가진 세포이며 red chlorophyll fluorescence (visible chlorophyll)가 관찰되면 HNFs로 간주하였다 (Round et al. 1990). HNFs와 protozooplankton (예: ciliates, amoebae)의 구별은 Patterson (2003)의 방법대로 접안렌즈 내의 calibrated ocular grid를 사용해 크기 별로 group화하여 분별해 주었다. 이 방법으로는 HNFs의 정확한 수를 계수할 수는 없지만, 샘플들 사이의 세포수 변화 경향을 확인할 수 있는 좋은 방법이다. 개별 flagellate의 크기는 calibrated ocular grid를 사용해 측정하였다. 식물플랑크톤의 계수를 위해 1 mL을 분취해 Sedgwick-Rafter counting chamber (PhycoTech Inc., USA)를 사용하여 200 magnification로 IX71 inverted microscope (Olympus, Japan) 하에서 계수하였다. 섬모충 (ciliates)과 동물플랑크톤 (zooplankton)의 계수를 위해 각각 1 L과 20 L를 농축한 샘플을 채수한 후 15 mL tube와 산 처리된 300 mL polyethylene bottle에 각각 담아 Lugol’s solution (final concentration 1%)과 formalin (final concentration 2%)으로 고정하였다 (Nakano et al. 1998). 동물플랑크톤은 샘플을 gridded slide 위에서 올린 후 적당한 배율 (40 ~ 400)의 IX71 inverted microscope 하에서 계수하였다.
2.5 Mesocosm (30 ton) 내 식물플랑크톤 종 다양성 분석
Mesocosm 내 NQ 2-0 접종 후 물질에 의한 식물플랑크톤 군집의 변화를 알아보기 위해 종 다양성 지수 (diversity index)를 산출하고자 하였다. NQ 2-0 물질을 적용하지 않은 대조구와 NQ 2-0 물질을 처리한 처리구에서 각각 산출하였으며, 종 다양성 지수의 경우 Margalef (1958)의 정보이론에 의해 유도된 Shannon- Wiever의 식 (Pielou 1969)을 이용하여 산출하였다.
Shannon-Wiener diversity index: H =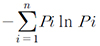
상기 식에서 H: 다양도, n: 전체 종 수, Pi: i 번째에 속하는 개체수의 비율을 의미하며, (ni/N)으로 계산 (N: 군집 내의 전체 현존량, ni: 각 종의 현존량)하는 것을 의미한다.
2.6 데이터 분석
살조물질에 의한 살조효과 또는 살조활성 (algicidal activity)은 다음 식으로 계산하였다.
Algicidal activity (%) = (1-Tt/Ct)×100,
이때 T (처리구)와 C (대조구)는 각각 NQ 2-0 물질이 접종되었을 때와 접종되지 않았을 때의 조류 세포수이며, t는 처리 기간 (day)수를 의미한다.
3. 결 과
3.1 Naphthoquinone 2-0 (NQ 2-0) 물질의 선택적 살조효과
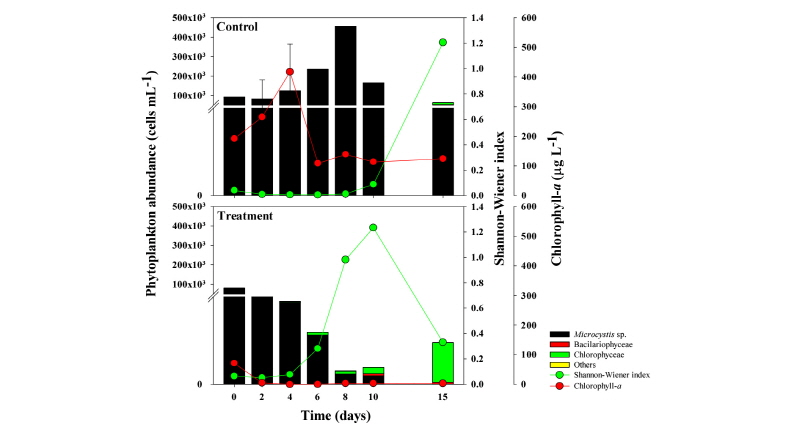
기흥저수지 현장에서 30 ton 규모의 mesocosm 실험 결과, 대조구에서는 대상 조류 Microcystis sp. 세포수가 초기 세포밀도 9.1×104 cells mL-1에서 실험 8일까지 지속적으로 성장하여 4.5×105 cells mL-1까지 세포수가 증가하였다 (Fig. 3). 이 후, 감소하기 시작하여 15일차 1.5×104 cells mL-1까지 감소하였다. 반면, NQ 2-0 물질을 접종한 처리구의 경우, 실험 초기 7.9×104 cells mL-1에서 접종 후 점진적으로 세포수가 감소하여 10일차 9.7×102 cells mL-1으로 대조구 대비 99.4% 감소하였다 (Fig. 3). 이 후, 실험 종료시인 15일차에는 대상 조류인 Microcystis sp. 세포수가 100% 제거되어 관찰되지 않았다. 실험기간 동안 대조구의 경우, 10일차까지 Microcystis sp. 종이 90% 이상 지속적으로 우점하였으며, 15일차에만 S. hantzschii 종이 우점하였다. 이외에 Ankistrodesmus falcatus, Nitzschia sp., Scenedesmus sp.와 같은 녹조류와 규조류가 대조구 및 처리구 모두에서 주로 출현하였다 (Fig. 3).
Mesocosm 내 Chlorophyll-a 변화를 관찰한 결과, 대조구에서는 실험초기 192.0 ± 50.8 µg L-1의 농도에서 4일차 417.2 ± 93.4 µg L-1까지 증가하였으나, 이 후 감소하여 실험 종료시인 15일차 124.2 ± 61.4 µg L-1까지 감소하였다 (Fig. 3). NQ 2-0 물질 처리구의 경우, 실험초기 70.9 ± 23.1 µg L-1에서 물질 접종 후 점진적으로 감소하여 15일차에는 2.9 ± 2.1 µg L-1까지 감소하였다 (Fig. 3).
3.2 Naphthoquinone 2-0 (NQ 2-0)의 mesocosm 내 적용 후 모니터링
3.2.1 비생물학적 요인의 변화
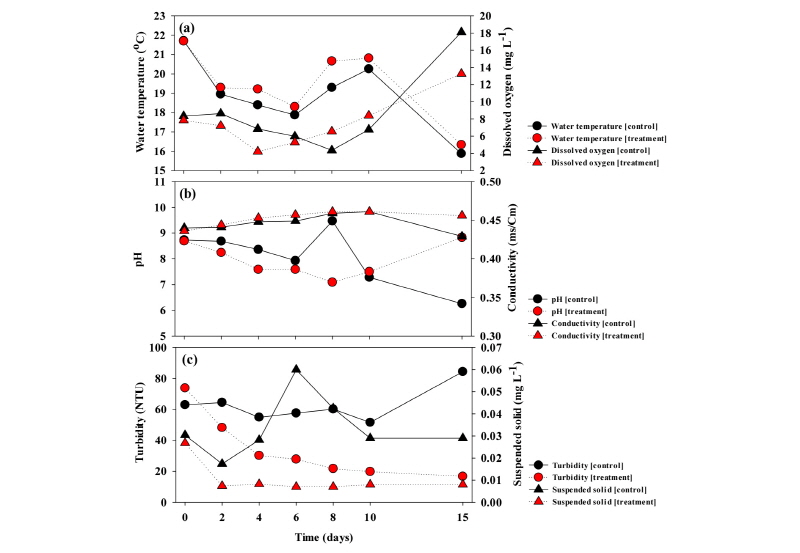
NQ 2-0 물질 접종 후 mesocosm 내 환경요인을 분석한 결과, 수온의 경우 실험초기 21.7°C에서 점진적으로 감소하여 15일차에는 대조구 15.8°C, 처리구 16.6°C로 관찰되었으며, 실험기간 동안 대조구, 처리구 모두 15.8 ~ 21.7°C 사이로 처리구와 대조구에서 유사한 경향으로 관찰되었다 (Fig. 4a). Mesocosm 내 용존 산소 농도는 실험 초기 대조구 8.3 mg L-1, 처리구 7.8 mg L-1 로 관찰되었으며, 10일차까지는 일정한 농도로 유지된 후 종료시인 15일차 대조구와 처리구 모두 18.1 mg L-1, 13.3 mg L-1으로 급증하였으나, 실험기간 동안 대조구와 처리구 모두 유사한 경향으로 관찰되었다 (Fig. 4a). pH의 경우 실험 초기 대조구 8.7, 처리구 8.6으로 관찰되었으며, 10일차까지 대조구, 처리구에서 7.2 ~ 9.4 사이의 범위로 큰 변화 없이 유사한 경향을 보였다 (Fig. 4b). 다만, 15일차에 대조구는 6.2, 처리구는 8.8으로 다소 차이가 보였다. 전기전도도는 대조구와 처리구에서 실험초기 각 0.440 mS/cm, 0.436 mS/cm에서 15일차 0.429 mS/cm, 0.456 mS/cm으로 큰 변화 없이 유지되었다 (Fig. 4b). Mesocosm 내 탁도의 경우, 대조구는 실험초기 63.0 NTU에서 점진적으로 증가하여 15일차 84.4 NTU까지 탁도가 증가하였다. 그러나, NQ 2-0 물질 처리구에서는 실험초기 73.8 NTU로 대조구보다 높았으나, 접종 2일차부터 점진적으로 감소하여 16.7 NTU로 낮게 측정되었으며 mesocosm 내 투명도가 개선되었다 (Fig. 4c). 또한, mesocosm 내 부유물질의 경우, 대조구는 실험초기 0.03 mg L-1에서 점진적으로 증가하여 6일차 0.06 mg L-1 까지 부유물질이 증가하였다가 이 후 다시 감소하여 15일차 0.029 mg L-1으로 관찰되었다. 그러나, NQ 2-0 물질 처리구에서는 실험초기 0.026 mg L-1에서 점진적으로 감소하여 0.008 mg L-1로 부유물질 역시 감소하였다 (Fig. 4c).
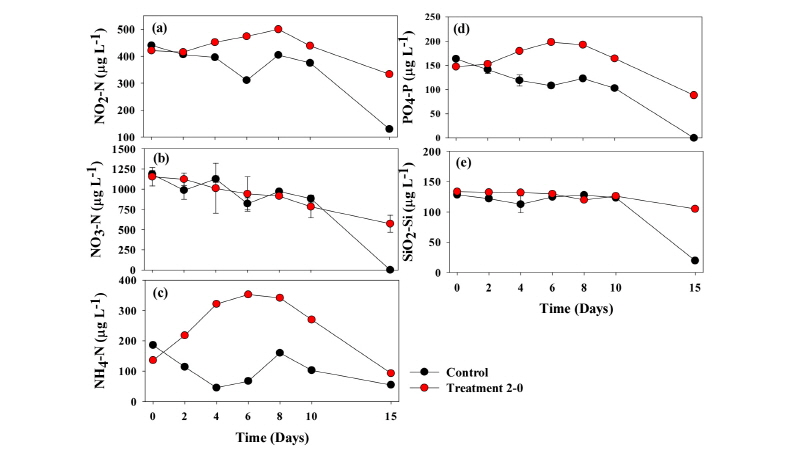
환경요인과 더불어 mesocosm 내 영양염의 변화를 관찰한 결과, 아질산성 질소 (NO2-N)의 경우 실험초기 대조구, 처리구 각 439.8 ± 5.8 µg L-1, 420.8 ± 0.4 µg L-1으로 관찰되었다. 그러나, 대조구의 경우 점진적으로 감소하여 15일차 129.5 ± 3.1 µg L-1까지 감소하였으나, 처리구에서는 8일차까지 증가하여 499.7 ± 1.8 µg L-1까지 증가 후 감소하여 15일차 332.9 ± 3.6 µg L-1으로 관찰되었다 (Fig. 5a). 질산성 질소 (NO3-N)의 경우, 실험초기 대조구, 처리구 각 1184.6 ± 45.0 µg L-1, 1154.6 ± 114.0 µg L-1으로 관찰되었다. 이 후 10일차까지 대조구와 처리구 모두 일정 농도를 유지하였으며, 15일차 대조구에서 급격하게 감소하는 경향을 보였다 (Fig. 5b). 암모니아성 질소 (NH4-N)의 경우, 실험초기 대조구와 처리구에서는 각각 185.7 ± 4.0 µg L-1, 135.7 ± 5.0 µg L-1으로 측정되었으며, 대조구의 경우 15일차까지 45.1 ~ 185.7 µg L-1 사이의 농도에서 유지되었다. 그러나, 처리구의 경우, 2일차부터 점진적으로 증가하여 6일차 352.6 ± 3.1 µg L-1까지 증가한 후 다시 감소하여 15일차에는 92.6 ± 6.8 µg L-1으로 관찰되었다 (Fig. 5c). 인산염인 (PO4-P)의 경우 실험초기 대조구와 처리구에서는 각각 163.4 ± 0.7 µg L-1, 147.3 ± 3.0 µg L-1으로 관찰되었다. 이 후 대조구의 경우 점진적으로 감소하여 10일차 102.8 ± 1.5 µg L-1까지 감소하였으며 15일차에는 검출되지 않았다 (Fig. 5d). 반면, 처리구의 경우 점진적으로 증가하여 6일차 198.0 ± 1.5 µg L-1 까지 증가하였다가 감소하여 15일차 88.2 ± 2.3 µg L-1으로 측정되었다 (Fig. 5d). 규산 규소 (SiO2-Si)의 경우, 실험초기 대조구와 처리구에서는 각각 128.3 ± 1.5 µg L-1, 133.3 ± 0.06 µg L-1으로 관찰되었다. 이 후 10일차까지 대조구와 처리구 모두 105.0 ~ 133.3 µg L-1 범위에서 유지되었으나, 15일차 대조구에서 19.6 ± 0.3 µg L-1으로 급격히 감소하는 경향을 보였다 (Fig. 5e)
3.2.2 생물학적 요인의 변화
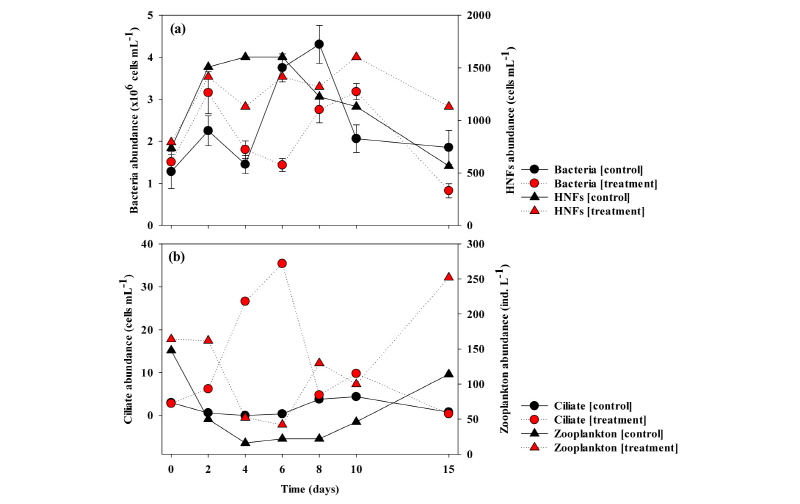
실험 초기 mesocosm 내 박테리아의 개체수는 대조구와 처리구 각각 (1.2 ± 0.4)×106 cells mL-1, (1.5 ± 0.2)×106 cells mL-1로 관찰되었다. 이 후 15일차까지 0.8×106 cells mL-1 ~ 4.3×106 cells mL-1 범위로 큰 변화 없이 모든 실험구에서 일정하게 유지되는 것을 확인할 수 있었다 (Fig. 6a). HNFs의 경우, 실험 초기 대조구, 처리구 각각 735.1 cells mL-1, 791.6 cells mL-1이었으나 점진적으로 증가하여 10일차 1130.9 cells mL-1, 1602.2 cells mL-1까지 증가하였다. 이 후 15일차에는 대조구와 처리구 모두 감소하여 각 565.4 cells mL-1, 1130.9 cells mL-1로 관찰되었다. 전체적으로 박테리아 변화와 유사하게 모든 실험구에서 큰 차이 없이 실험기간 동안 565.4 ~ 1602.2 cells mL-1 범위 내에서 관찰되었다 (Fig. 6a).
전체적인 식물플랑크톤 개체수는 대조구 실험초기 9.1×104 cells mL-1에서 8일차까지 점진적으로 증가하여 4.5×105 cells mL-1까지 증가한 후 감소하는 경향을 보였다. 그러나, 초기 8.0×104 cells mL-1 세포 밀도였던 처리구에서는 15일차 4.7×103 cells mL-1으로 우점종인 Microcystis sp. 종의 감소에 의한 전체 식물플랑크톤이 감소되었다 (Fig. 3). Mesocosm 내 섬모충의 경우, 대조구와 처리구 모두 실험초기 3.0 cells mL-1, 2.0 cells mL-1 개체수가 관찰되었다. 그러나, 대조구의 경우 실험 종료시인 15일차까지 낮은 개체수로 유지된 반면, 처리구의 경우 6일차까지 급진적으로 개체수가 증가하여 35.4 cells mL-1까지 증가하였다가 다시 감소하는 경향을 나타내었다 (Fig. 6b). 동물플랑크톤의 경우, 대조구와 처리구에서 험초기 148.0 individual L-1, 164.0 individual L-1 개체수가 관찰되었으며, 실험기간 동안 대조구보다 처리구에서 높은 개체수가 유지되었다 (Fig. 6b).
4. 고 찰
녹조현상을 제어하기 위해 다방면에서 기술이 개발되었으나, 높은 살조효과, 빠른 제어효율, 편의성 등의 장점으로 화학적 제어물질을 이용한 녹조제어 기술이 현장적용의 가능성이 가장 높다고 평가되고 있다. 더구나, 화학적 제어물질 중에 저독성, 빠른 분해 등의 친환경적 특징을 갖고 있는 생물 유래 물질을 이용한 기술이 각광받고 있다. 본 연구에서 사용한 naphthoquinone은 역시 식물 (Diospyros ebenum, Impatiens balsamina etc.) 및 미생물 (Streptococcus faecalis etc.) 내 존재하는 천연물로서, 다양한 기능을 갖고 있어 의약품 (medical supplies), 제초제 (herbicide), 살균제 (antimicrobial agent) (O’Brien 1991, Monks et al. 1992, Schrader et al. 2003, Dong et al. 2009) 등으로 사용되고 있는 물질이다. 더불어 최근에는 이러한 기능을 바탕으로 유해 남조류 및 규조류 제어를 위한 살조물질로 연구되어 그 효능이 입증되었다 (Byun et al. 2015, Joo et al. 2016a, Joo et al. 2017). 또한, NQ 유도체의 경우, 대상 조류만을 선택적으로 제어 가능하며, 생태독성 지표 생물 대하여 현장 적용 농도에서 독성이 없다고 보고되었다 (Joo et al. 2016b, Joo et al. 2017). 그러나, 실험실 내의 높은 살조효과와 저독성의 결과만으로는 실제 수계 적용시 동일한 효과를 장담할 수 없다. 실제로 기존에 개발된 다양한 녹조제어 기술들 대부분은 실험실에서 수행되는 소규모 실험에서는 대상 조류의 제어효과를 입증하였으나, 실험구의 처리 용량이 커지거나 실제 수계에서는 다양한 요인에 의해 제어 효과가 미미한 경우가 빈번히 발생하였다 (Schrader et al. 2003). 따라서, 개발된 살조물질의 현장 적용에 앞서, 현장에 존재하는 대상 남조류의 제어 가능 유무과 다양한 요인의 모니터링을 통한 현장 적용 가능성을 평가하는 것이 반드시 필요하다.
NQ 유도체의 경우 선행연구를 통하여 유해 조류에 대하여 선택적인 살조효과가 입증되었으나 (Joo et al. 2016b), 상기 결과는 실험실에서 유해 조류를 포함한 다양한 조류를 이용하여 살조효과의 유무를 파악함으로서 선택적 제어를 파악한 결과이다. 그러나, 조류 제어를 위한 살조물질의 적용은 실제 수중 내에서 대상 조류와 살조물질간의 단순한 1:1 관계만을 고려하기 어려우며, 다양한 요인과의 상호관계를 고려하지 않고 적용한다는 것은 매우 부정적인 결과를 얻기 쉽다. 즉, 현장에서의 결과 없이 실험실에서 얻은 결과만으로 현장 생태계에 적용한다면 좋은 결과를 얻기가 쉽지 않을 것이다 (Prieto et al. 2002, Pilkaityte et al. 2004). 더구나, 실험실 내 실험 혹은 소규모의 microcosm 실험에서는 높은 살조효과과 재현성을 갖는 살조물질이라 하더라도, 처리 용량이 커질수록 살조효과의 감소, 대상 조류의 재발생 등이 발생하였다 (Kaya et al. 2005). 특히, 여름철 대발생하여 가장 큰 문제를 일으키는 원인 종인 유해 남조류 Microcystis sp.의 경우, 실험실 내에서 장기간 배양을 통해 단일 세포형태 (single cell)로 존재할 때와는 달리, 현장 수계에서는 군체 (colony)형태로 존재하며 점막 (mucous)형성을 통해 수계 내 환경 조건에 의한 변화 및 섭식생물 등의 영향을 최소화할 수 있기 때문에 효과적인 제어가 어려운 실정이다. 더구나, 최근 전세계적으로 생물 종 다양성 (species diversity)에 대한 중요성이 부각되고 있는 실정이며, 국내 역시 수질개선에 대한 개념이 물리화학적 수질개선에서 생태적으로 건강한 수질개선으로 변화하고 있는 추세로 보다 친환경적인 살조물질 개발이 요구되고 있다 (Kim et al. 2008, Hong 2014). 본 연구에서 수행된 mesocosm 실험에서는 NQ 2-0 물질의 선택적 제어뿐만 아니라, 다양한 식물플랑크톤이 존재하는 수계에서 핵심종 (keystone species)였던 Microcystis sp. 종만을 제어함으로서, 식물플랑크톤의 종간경쟁 (interspecific com-petition)에서 뒤쳐져 있던 다양한 식물플랑크톤이 성장이 가능한 환경을 제공하였고, Scenedesmus sp., Stephanodiscus hantzschii 등의 다른 조류의 성장을 가능하게 하였다. 이러한 다른 조류의 성장으로 인해 수 생태계 건강성 지표인 생물 종 다양성 지수 (Shannon- Wiener diversity index)도 높아짐을 확인하였다 (Fig. 3). 종 다양성 지수의 증진 결과는 단순한 조류제어뿐만 아니라, 수 생태계의 건강성이 복원 및 증진된 것을 확인할 수 있는 결과로서, NQ 2-0 물질의 적용은 남조류 제어와 더불어 수계에 긍정적인 영향을 미칠 것으로 사료된다.
현장 조건에서의 선택적 살조효과과 더불어 NQ 2-0 물질의 수 생태계 미치는 영향을 평가하기 위해 기흥저수지 수변에 30 ton 규모의 mesocosm 설치 후, 물질을 적용하여 다양한 요인을 모니터링 하였다. 비생물학적 요인의 경우, 수온, 용존 산소, pH (15일차 제외)에서 대조구와 처리구에서 큰 차이없이 유사한 경향이 관찰되었다. 다만 15일차 pH의 경우, 대조구에서 다소 낮게 측정되었다. 이러한 결과는 대조구 내 Microcystis sp. 포함한 전체 식물플랑크톤 현존량이 급격하게 사멸됨에 따라 발생하는 용존 유기물질 (dissolved organic matter)과 박테리아 활성에 따라 낮게 관찰된 것으로 판단된다 (Baek et al. 2013, Jung et al. 2008, 2009, Joo et al. 2016a). 탁도와 부유물질의 경우, 대조구에서는 실험 초기부터 종료시까지 일정하게 유지되었으나, NQ 2-0 물질을 처리한 처리구에서는 적용 후 지속적으로 감소하였다 (Fig. 4c). 이러한 결과는 NQ 2-0 물질에 의해 Microcystis sp. 현존량이 급감하면서 mesocosm 내 탁도와 부유물질이 개선된 것으로 사료된다. 영양염 중에 아질산성 질소 (NO2-N), 암모니아성 질소 (NH4-N)과 인산염 인 (PO4-P)은 NQ 2-0 물질의 적용 후 실험 초기 대조구 대비 처리구에서 높게 측정되었다 (Fig. 5). 이는 우점종이었던 Microcystis sp.종이 NQ 2-0 물질에 의해 사멸되면서 세포로부터 용출되는 영양염에 의해 일시적으로 높은 농도가 측정된 것으로 판단되나 현장에서의 변화 가능한 범위 내에서의 유동적인 변화로서 생태계 미치는 영향은 없을 것이라 판단된다. 이를 제외한 질산성 질소 (NO3-N), 규산 규소 (SiO2-Si)의 경우 대조구와 처리구 모두 유사한 경향이 관찰되었다. 이러한 결과는, 기존의 살조제, 응집제 등의 현장 적용 후 영양염 재 용출에 의한 부영양화 촉진의 문제점이 (Hickey and Gibbs 2009) 발생하지 않는 물질로서 생태계 교란을 최소화한 기술로 사용이 가능할 것으로 판단된다.
NQ 2-0의 mesocosm 내 적용 후 박테리아와 HNFs의 개체수는 큰 변화없이 대조구와 처리구에서 유사한 경향을 보였다 (Fig. 6a). 그러나, 섬모충과 동물플랑크톤의 경우, 대조구 대비 처리구에서 높은 개체수를 보였다. 특히, 섬모충의 경우 NQ 2-0 접종 후 2일차부터 개체수가 증가하기 시작하여 6일차 35.4 cells mL-1까지 증가하였다. 이 후 8일차부터는 동물플랑크톤의 개체수가 증가하기 시작하여 15일차 252.0 individual L-1까지 증가하였다 (Fig. 6b). 이러한 결과는 실험초기 mesocosm 내 microcystin과 같은 조류 독성을 갖는 유해 남조류인 Microcystis sp. 종이 우점하였으나, NQ 2-0 물질에 의해 선택적으로 제어됨에 따라 상대적으로 선호하는 무독성의 조류가 성장하면서 섬모충과 동물플랑크톤의 풍부한 먹이원 공급으로 작용하여 개체수가 증가하는 현상이 관찰된것으로 판단된다. 이러한 동물플랑크톤의 성장은 2차적으로 발생한 녹조현상을 제어함으로써, 물질의 영향이 아닌 생물학적 녹조제어 (bioremediation)를 유발하는 역할을 하였다. 동물플랑크톤에 의한 2차적 조류 제어 기작은 대상 조류의 재발생없이 제어효과를 장기간 지속할 수 있도록 유도한것으로 사료된다. 즉, NQ 2-0 물질을 이용한 녹조제어 기술의 현장 적용은 단순한 유해 조류의 제어효과뿐만 아니라, 수생 생물의 서식처 및 먹이 공급을 원활하게 함으로써 전반적인 건강한 수 생태계를 형성하는데 큰 역할을 할 것으로 판단된다.
5. 결 론
여름철 유해 조류 대발생에 의한 피해를 막고자 개발된 NQ 2-0 물질은 30 ton 규모의 mesocosm 실험에서 대상 조류인 Microcystis sp. 종만을 99% 이상 선택적으로 제어하였으며, Microcystis sp. 종의 사멸에 따른 다른 조류가 성장할 수 있는 환경을 제공하였다. Micro-cystis sp. 종의 선택적 제어에 따른 식물플랑크톤 종 다양성 지수도 증가하였다. 뿐만 아니라, NQ 2-0 물질에 의해 생물학적, 비생물학적 요인에 미치는 영향이 없음을 확인하였다. 더불어, 30 ton 규모 mesocosm 실험을 통해 Microcystis sp. 만을 99% 이상 제어 가능함으로서 현장 적용 가능성을 입증하였으며, 기존 녹조제어 기술의 문제점이었던 적용 규모가 커짐에 따라 불안정한 살조효과의 문제를 해결하였다. 이러한 결과를 비추어 볼 때, NQ 2-0 물질을 이용한 녹조제어 기술은 현장에서도 높은 살조효과를 나타낼 수 있는 기술로서 현재까지 개발된 생물유래 물질 중 가장 효율적으로 적용 할 수 있는 물질이라고 생각된다.